પ્રતિક્રિયાઓનું પ્રથમ જૂથ અવેજીની પ્રતિક્રિયાઓ છે. અમે કહ્યું હતું કે એરેન્સ પરમાણુ માળખામાં બહુવિધ બોન્ડ્સ નથી, પરંતુ તેમાં છ ઇલેક્ટ્રોનની કન્જેક્ટેડ સિસ્ટમ છે, જે ખૂબ જ સ્થિર છે અને બેન્ઝિન રીંગને વધારાની શક્તિ આપે છે. તેથી, રાસાયણિક પ્રતિક્રિયાઓમાં, સૌ પ્રથમ, હાઇડ્રોજન અણુની ફેરબદલ થાય છે, અને બેન્ઝિન રિંગનો વિનાશ નહીં.
અલકેન્સ વિશે વાત કરતી વખતે આપણે પહેલાથી જ અવેજી પ્રતિક્રિયાઓનો સામનો કરવો પડ્યો છે, પરંતુ તેમના માટે આ પ્રતિક્રિયા એક આમૂલ મિકેનિઝમ અનુસાર આગળ વધી છે, જ્યારે એરેન્સને અવેજીના પ્રતિક્રિયાઓની આયનીય પદ્ધતિ દ્વારા વર્ગીકૃત કરવામાં આવે છે.
પહેલુંરાસાયણિક સંપત્તિ - હેલોજેનેશન. ક્લોરિન અથવા બ્રોમિન - હેલોજન અણુ માટે હાઇડ્રોજન અણુની અવેજી.
પ્રતિક્રિયા ગરમી સાથે અને હંમેશાં ઉત્પ્રેરકની ભાગીદારી સાથે આગળ વધે છે. ક્લોરિનના કિસ્સામાં, આ એલ્યુમિનિયમ ક્લોરાઇડ અથવા ફેરીક ક્લોરાઇડ ત્રણ હોઈ શકે છે. ઉત્પ્રેરક હેલોજન અણુનું ધ્રુવીકરણ કરે છે, પરિણામે હેટરોલિટીક બોન્ડ ક્લિવેજ અને આયન થાય છે.
સકારાત્મક ચાર્જ ક્લોરિન આયન અને બેન્ઝીન સાથે પ્રતિક્રિયા આપે છે.
જો પ્રતિક્રિયા બ્રોમાઇન સાથે થાય છે, તો પછી ઉત્પ્રેરક ફેરીક બ્રોમાઇડ અથવા એલ્યુમિનિયમ બ્રોમાઇડ છે.

એ નોંધવું મહત્વપૂર્ણ છે કે પ્રતિક્રિયા મોલેક્યુલર બ્રોમિન સાથે થાય છે, બ્રોમિન પાણીથી નહીં. બzનઝિન બ્રોમિન પાણીથી પ્રતિક્રિયા આપતું નથી.
બેન્ઝીન હોમોલોગ્સનું હloલોજેનેશન તેની પોતાની લાક્ષણિકતાઓ છે. ટોલ્યુએન પરમાણુમાં, મિથાઈલ જૂથ રિંગમાં અવેજીની સુવિધા આપે છે, પ્રતિક્રિયાશીલતા વધે છે, અને પ્રતિક્રિયા હળવા શરતો હેઠળ આગળ વધે છે, એટલે કે પહેલાથી ઓરડાના તાપમાને.

એ નોંધવું મહત્વપૂર્ણ છે કે અવેજી હંમેશા substર્થો અને પેરા સ્થાનો પર થાય છે, તેથી આઇસોમર્સનું મિશ્રણ મેળવવામાં આવે છે.
બીજુંપ્રોપર્ટી - બેન્ઝિનનું નાઇટ્રેશન, બેન્ઝીન રિંગમાં નાઇટ્રો જૂથનો પરિચય.
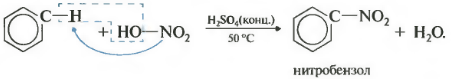
કડવી બદામની ગંધ સાથે એક પીળો રંગનો ભારે પ્રવાહી રચાય છે - નાઇટ્રોબેન્ઝિન, તેથી પ્રતિક્રિયા બેંઝિનની ઉચ્ચ ગુણવત્તાની હોઈ શકે છે. નાઈટ્રેશન માટે, કેન્દ્રિત નાઇટ્રિક અને સલ્ફ્યુરિક એસિડ્સના નાઇટ્રેટિંગ મિશ્રણનો ઉપયોગ થાય છે. પ્રતિક્રિયા ગરમી સાથે કરવામાં આવે છે.
હું તમને યાદ કરાવું કે કોનોવલોવની પ્રતિક્રિયામાં એલ્કેન્સના નાઇટ્રેશન માટે, અમે સલ્ફ્યુરિક એસિડ ઉમેર્યા વિના પાતળા નાઈટ્રિક એસિડનો ઉપયોગ કર્યો છે.
ટોલ્યુઇનના નાઇટ્રેશન દરમિયાન, તેમજ હેલોજેનેશન દરમિયાન, ઓર્થો અને પેરા આઇસોમર્સનું મિશ્રણ રચાય છે.

ત્રીજુંપ્રોપર્ટી - હloલોકkanનેસ સાથે બેન્ઝિનનું આલ્કિલેશન.

આ પ્રતિક્રિયા બેંઝિન રિંગમાં હાઇડ્રોકાર્બન રેડિકલ દાખલ કરવાની મંજૂરી આપે છે અને બેન્ઝિન હોમોલોગ્સ મેળવવાનો માર્ગ માનવામાં આવે છે. એલ્યુમિનિયમ ક્લોરાઇડનો ઉપયોગ ઉત્પ્રેરક તરીકે થાય છે, જે હેલોલકેન પરમાણુના સડોને આયનોમાં પ્રોત્સાહન આપે છે. ગરમી પણ જરૂરી છે.
ચોથુંપ્રોપર્ટી - એલ્કેનેસ સાથે બેન્ઝિનનું આલ્કિલેશન.
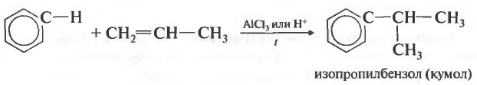
આ રીતે, તમે મેળવી શકો છો, ઉદાહરણ તરીકે, ક્યુમેન અથવા ઇથિલબેન્ઝિન. ઉત્પ્રેરક એલ્યુમિનિયમ ક્લોરાઇડ છે.
2. બેન્ઝીન ઉપરાંતની પ્રતિક્રિયાઓ
પ્રતિક્રિયાઓનું બીજું જૂથ એ વધારાની પ્રતિક્રિયાઓ છે. અમે કહ્યું હતું કે આ પ્રતિક્રિયાઓ લાક્ષણિક નથી, પરંતુ પાઇ-ઇલેક્ટ્રોન વાદળના વિનાશ અને છ સિગ્મા બોન્ડ્સની રચના સાથે કડક પરિસ્થિતિઓ હેઠળ તે શક્ય છે.
પાંચમુંસામાન્ય સૂચિમાં ગુણધર્મ - હાઇડ્રોજન, હાઇડ્રોજનનો ઉમેરો.
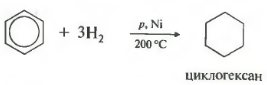
તાપમાન, દબાણ, ઉત્પ્રેરક નિકલ અથવા પ્લેટિનમ. ટોલુએન એ જ રીતે પ્રતિક્રિયા આપી શકે છે.
છઠ્ઠામિલકત - ક્લોરીનેશન. કૃપા કરીને નોંધો કે અમે કલોરિન સાથેની ક્રિયાપ્રતિક્રિયા વિશે ખાસ વાત કરી રહ્યા છીએ, કારણ કે બ્રોમિન આ પ્રતિક્રિયામાં પ્રવેશતું નથી.
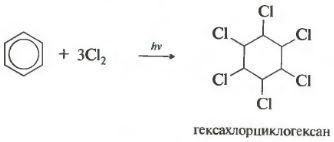
આ પ્રતિક્રિયા ગંભીર અલ્ટ્રાવાયોલેટ કિરણોત્સર્ગમાં થાય છે. રચાયેલ હેક્સાચલોરોસાયક્લોહેક્ઝેન, બીજું નામ હેક્સાચ્લોરેન છે, એક નક્કર.
તે યાદ રાખવું અગત્યનું છે કે બેન્ઝીન માટે શક્ય નથી હાઇડ્રોજન હાયલાઇડ્સ (હાઇડ્રોહેલોજેનેશન) અને પાણી (હાઇડ્રેશન) ના ઉમેરાની પ્રતિક્રિયાઓ.
3. બેન્ઝિન હોમોલોગ્સની સાઇડ સાંકળમાં અવેજી
પ્રતિક્રિયાઓનો ત્રીજો જૂથ ફક્ત બેન્ઝિન હોમોલોગ્સની ચિંતા કરે છે - આ બાજુ સાંકળનો અવેજી છે.
સાતમુંસામાન્ય સૂચિમાં ગુણધર્મ - બાજુ સાંકળમાં આલ્ફા કાર્બન અણુમાં હેલોજેનેશન.
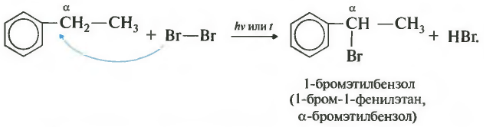
પ્રતિક્રિયા ત્યારે થાય છે જ્યારે ગરમ થાય છે અથવા ઇરેડિયેટ થાય છે, અને હંમેશા ફક્ત આલ્ફા કાર્બન પર. જેમ જેમ હેલોજેનેશન ચાલુ છે, તેમ તેમ બીજા હેલોજન અણુ આલ્ફા સ્થિતિમાં પાછા આવશે.
4. બેન્ઝિન હોમોલોગ્સનું Oxક્સિડેશન
પ્રતિક્રિયાઓનો ચોથો જૂથ idક્સિડેશન છે.
બેન્ઝિન રિંગ ખૂબ મજબૂત છે, તેથી બેન્ઝિન ઓક્સિડાઇઝ કરતું નથી પોટેશિયમ પરમેંગેનેટ - તેના સોલ્યુશનને વિકૃત કરતું નથી. આ યાદ રાખવું ખૂબ જ મહત્વપૂર્ણ છે.
પરંતુ બેન્ઝિનના હોમોલોગ્સ જ્યારે ગરમ થાય છે ત્યારે પોટેશિયમ પરમેંગેનેટના એસિડિફાઇડ સોલ્યુશન દ્વારા ઓક્સિડાઇઝ્ડ કરવામાં આવે છે. અને આ આઠમી રાસાયણિક સંપત્તિ છે.
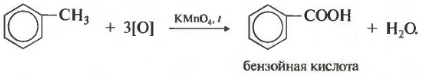
તે બેન્ઝોઇક એસિડ બહાર કા .ે છે. સોલ્યુશનની વિકૃતિકરણ અવલોકન કરવામાં આવે છે. આ કિસ્સામાં, અવેજીની કાર્બન સાંકળ કેટલી લાંબી છે, તે હંમેશાં પ્રથમ કાર્બન અણુ પછી તૂટી જાય છે અને બેન્ઝોઇક એસિડની રચના સાથે આલ્ફા અણુ કાર્બોક્સિલ જૂથમાં ઓક્સિડાઇઝ્ડ થાય છે. બાકીના પરમાણુ સંબંધિત એસિડમાં ઓક્સિડાઇઝ્ડ થાય છે અથવા, જો તે માત્ર એક જ કાર્બન અણુ હોય તો કાર્બન ડાયોક્સાઇડમાં.
જો બેન્ઝિન હોમોલોગમાં સુગંધિત રિંગ પર એક કરતા વધુ હાઇડ્રોકાર્બન પદાર્થ હોય, તો ઓક્સિડેશન તે જ નિયમો અનુસાર આગળ વધે છે - આલ્ફા પોઝિશનમાં કાર્બનનું ઓક્સિડેશન થાય છે.

આ ઉદાહરણ ફિથાલિક એસિડ તરીકે ઓળખાતું ડિબેસિક સુગંધિત એસિડ ઉત્પન્ન કરે છે.
સલ્ફ્યુરિક એસિડની હાજરીમાં વાતાવરણીય ઓક્સિજન દ્વારા હું ખાસ કરીને ક્યુમિન, આઇસોપ્રોપીલબેન્ઝિનના oxક્સિડેશનની નોંધ લઈશ.

ફેનોલ ઉત્પન્ન કરવા માટેની આ કહેવાતી ક્યુમિન પદ્ધતિ છે. એક નિયમ તરીકે, કોઈએ ફેનોલના ઉત્પાદન સાથે સંબંધિત બાબતોમાં આ પ્રતિક્રિયા સાથે વ્યવહાર કરવો પડશે. આ anદ્યોગિક માર્ગ છે.
નવમીસંપત્તિ - દહન, oxક્સિજન સાથે સંપૂર્ણ idક્સિડેશન. બેન્ઝિન અને તેના હોમોલોગ્સ કાર્બન ડાયોક્સાઇડ અને પાણીને બાળી નાખે છે.
ચાલો સામાન્ય સ્વરૂપમાં બેન્ઝીન કમ્બશનનું સમીકરણ લખો.
સમૂહ સંરક્ષણના કાયદા અનુસાર, ડાબી બાજુએ એટલા જ જમણા પરમાણુ હોવા જોઈએ. કેમ કે રાસાયણિક પ્રતિક્રિયાઓમાં અણુ અદૃશ્ય થઈ જતા નથી, પરંતુ તેમની વચ્ચેના બોન્ડ્સનો ક્રમ ફક્ત બદલાઇ જાય છે. તેથી ત્યાં ઘણા કાર્બન ડાયોક્સાઇડ પરમાણુ હશે કારણ કે એરેન પરમાણુમાં કાર્બન અણુ હોય છે, કારણ કે પરમાણુમાં એક કાર્બન અણુ હોય છે. તે છે, n CO 2 અણુઓ. જળના અણુઓ હાઈડ્રોજન અણુ જેટલા અર્ધ જેટલા હશે, એટલે કે (2 એન -6) / 2, જેનો અર્થ થાય છે એન -3.
ડાબી અને જમણી બાજુના oxygenક્સિજન અણુ સમાન સંખ્યા છે. જમણી બાજુએ, કાર્બન ડાયોક્સાઇડના 2n છે, કારણ કે દરેક પરમાણુમાં 3 ઓક્સિજન અણુ હોય છે, વત્તા એન -3 પાણીથી, કુલ 3n-3. ડાબી બાજુ, ત્યાં સમાન સંખ્યામાં oxygenક્સિજન અણુઓ છે - 3 એન -3, જેનો અર્થ છે કે ત્યાં અડધા પરમાણુઓ છે, કારણ કે પરમાણુમાં બે અણુ હોય છે. તે છે (3 એન -3) / 2 ઓક્સિજન પરમાણુઓ.
આમ, આપણે બેન્ઝિન હોમોલોગ્સ માટેના કમ્બશન ઇક્વેશનને સામાન્ય સ્વરૂપમાં કમ્પાઇલ કર્યું છે.
PRTSVSH (F) FGBOU VPO
"ફાયર સેફ્ટી" વિભાગ
કસોટી
શિસ્તમાં "દહન અને વિસ્ફોટોનો થિયરી"
કાર્ય નંબર 1
બેન્ઝિન વરાળના સંપૂર્ણ દહન માટે જરૂરી ચોક્કસ સૈદ્ધાંતિક રકમ અને હવાના જથ્થાને નિર્ધારિત કરો. તાપમાન ટીજી અને દબાણ પીડબ્લ્યુ, અને બેન્ઝિન વરાળ - તાપમાન ટીજી અને પ્રેશર પીજી દ્વારા હવા કે જે સ્થિતિમાં સ્થિત છે તે લાક્ષણિકતાઓ છે. નીચેના એકમોમાં ગણતરીના પરિણામો દર્શાવો:; ;;;
પ્રારંભિક ડેટા (એન - જૂથ નંબર, એન - નંબર વિદ્યાર્થીઓની સૂચિ અનુસાર:
ટીવી \u003d 300 + (- 1) એન * 2 * એન - (- 1) એન * 0.2 * એન \u003d 277.6 કે
Рв \u003d? 10 3 \u003d 95900 પા;
ટીજી \u003d 300? (? 1) એન? 2? એન? (? 1) એન? 0.2? એન \u003d 321.6 કે;
પ્ર \u003d? 10 3 \u003d 79400 પા.
C6H6 + 7.5O2 + 7.5? 3.76N2 \u003d 6CO2 + 3pO + 7.5? 3.76N2 + Qp (1),
જ્યાં Qр એ રાસાયણિક પ્રતિક્રિયાની ગરમી છે. આ સમીકરણથી, બેન્ઝીન અને મોલેક્યુલર oxygenક્સિજનના સ્ટichચિઓમેટ્રિક ગુણાંક નક્કી કરી શકાય છે: વીજી \u003d 1, વી 0 \u003d 7.5
2. હવાની વિશિષ્ટ સૈદ્ધાંતિક માત્રા - બેંઝિનના એક કિલોમોલના સંપૂર્ણ દહન માટે જરૂરી હવાના કિલોમોલની સંખ્યા, સૂત્ર દ્વારા ગણતરી કરવામાં આવે છે:
જ્યાં 76.7676 એ ઓક્સિજનના એકમ ધરાવતા હવાના જથ્થા છે, \u003d તે પરમાણુ ઓક્સિજન (વી) અને બેન્ઝિન (વીજી) ના સ્ટichચિઓમેટ્રિક ગુણાંકનો ગુણોત્તર છે
(ડી) Vо અને Vg ના મૂલ્યોમાં ફેરબદલ, અમે મેળવીએ છીએ:
3. એક કિલોમોલ બેન્ઝિનના સંપૂર્ણ દહન માટે જરૂરી હવાનું પ્રમાણ નીચે મુજબ નક્કી કરવામાં આવે છે:
તાપમાન ટીવી અને પ્રેશર પીડબ્લ્યુ પર એક કિલોમીલ હવાનું પ્રમાણ ક્યાં છે. સૂત્રનો ઉપયોગ કરીને મૂલ્યની ગણતરી કરવામાં આવે છે
જ્યાં 22.4 એ સામાન્ય પરિસ્થિતિમાં ગેસનું દાળનું પ્રમાણ છે, પો \u003d 101325 પા - સામાન્ય દબાણ, તો \u003d 273 કે - સામાન્ય તાપમાન.
ટીવી, ટુ, પીબી, પો ઇન (5) ની જગ્યાએ, અમે મેળવીએ છીએ
સૂત્ર (4) દ્વારા ચોક્કસ સૈદ્ધાંતિક હવાના પ્રમાણની ગણતરી કરવામાં આવે છે:
G. વાયુયુક્ત બળતણના વોલ્યુમના એકમના સંપૂર્ણ દહન માટે જરૂરી હવાના જથ્થાને નીચે પ્રમાણે નક્કી કરવામાં આવે છે:
તાપમાન ટી.જી. અને પ્રેશર પી.જી. પર બેન્ઝિન વરાળ - એક કિલોમોલ ઇંધણનું પ્રમાણ ક્યાં છે. તે ધ્યાનમાં લેતા
અને ()) માં ()) અને ()) બદલીને, અમે હવાના વિશિષ્ટ સૈદ્ધાંતિક વોલ્યુમ માટે નીચેની અભિવ્યક્તિ પ્રાપ્ત કરીએ છીએ:
અમે દહન પ્રક્રિયાના આ પરિમાણની કિંમતની ગણતરી કરીએ છીએ:
એક કિલોગ્રામ બેન્ઝિનના સંપૂર્ણ દહન માટે જરૂરી હવાનું પ્રમાણ નીચે મુજબ નક્કી કરવામાં આવે છે:
ઇંધણનો દાળનો માસ ક્યાં છે - એક કિલોમોલ બેન્ઝિનનો સમૂહ, કિલોગ્રામમાં વ્યક્ત થાય છે. બેન્ઝીનના દાolaનો સમૂહ આંકડાકીય રીતે તેના પરમાણુ વજનની સમાન છે, તે સૂત્ર દ્વારા મળી:
AC? Nc + An? Nn, UiAi? Ni (11)
જ્યાં એસી અને એન કાર્બન અને હાઇડ્રોજનનું અણુ વજન છે, ત્યાં એનસી અને એન બેંઝિન પરમાણુમાં કાર્બન અણુઓની સંખ્યા છે. એસી \u003d 12, એનસી \u003d 6, એન \u003d 1, એનн \u003d 6 ની કિંમતોનો બદલો, અમે મેળવીએ છીએ:
આપણે સૂત્ર (10) માં એનના મૂલ્યોને બદલીને હવાના વિશિષ્ટ સૈદ્ધાંતિક વોલ્યુમને શોધીએ છીએ:
ગણતરી પરિણામ:
કાર્ય નંબર 2
બેન્ઝિન કમ્બશન ઉત્પાદનોની ચોક્કસ સૈદ્ધાંતિક રકમ, વોલ્યુમ અને રચના નક્કી કરો, જો વધારે હવાનું પ્રમાણ temperature, તાપમાન ટી.પી. અને દબાણ પીપી, કમ્બશન ઉત્પાદનોનો તાપમાન ટી.જી. અને પ્રેશર પી.જી. જાણીતા છે. ગણતરીના પરિણામો દાola અપૂર્ણાંક (ટકામાં) અને નીચેના એકમોમાં વ્યક્ત કરવામાં આવશે:; ;;
પ્રારંભિક ડેટા:
સી \u003d 1.5 + (? 1) એન? 0.1? એન? (? 1? એન? 0.01? એન \u003d 0.2;
પીપી \u003d? 10 3 \u003d 68400 પા;
Тп \u003d 1600? (? 1) એન? 20? એન? (? 1) એન? 2? એન \u003d 1816 કે;
ટીજી \u003d 273? (? 1) એન? 2? એન + (? 1) એન? 0.2? એન \u003d 295.4 કે;
પ્ર \u003d? 10 3 \u003d 111600 પા;
સોલ્યુશન (એન \u003d 11, એન \u003d 2).
1. ચાલો હવામાં બેંઝિન કમ્બશનની પ્રતિક્રિયાનું સ્ટichચિઓમેટ્રિક સમીકરણ લખો:
С 6 Н 6 + 7.5О 2 +7.5? 3.76N 2 \u003d 6CO 2 + 3H 2 O + 7.5? 3.76N 2 + Qp, (1)
જ્યાં ક્યુપી એ રાસાયણિક પ્રતિક્રિયાની ગરમી છે. આ સમીકરણથી, અમે નીચેના સ્ટichચિઓમેટ્રિક ગુણાંક નક્કી કરીએ છીએ:
વી સીઓ 2 \u003d 6, વી પીઓ \u003d 3, વી સી 6 એચ 6 \u003d 1, વી ઓ 2 \u003d 7.5, વી એન 2 \u003d 7.5? 3.76
2. એક કિલોમોલ ઇંધણના દહન ઉત્પાદનોની અંદાજિત રકમ નક્કી કરો:
(2) દહન ઉત્પાદનો અને બળતણના સ્ટ fuelચિઓમેટ્રિક ગુણાંકના મૂલ્યોમાં ફેરબદલ, અમે મેળવીએ છીએ:
Air. હવાના વિશિષ્ટ સૈદ્ધાંતિક જથ્થા - એક કિલોગ્રામ ઇંધણના સંપૂર્ણ દહન માટે જરૂરી હવાના કિલોમોલની સંખ્યા, સૂત્રનો ઉપયોગ કરીને નક્કી કરવામાં આવશે:
જ્યાં 76.7676 એ હવાનો જથ્થો છે જેમાં ઓક્સિજનનું એકમ હોય છે,
પરમાણુ oxygenક્સિજન અને બેન્ઝિનના સ્ટichચિઓમેટ્રિક ગુણાંકનો ગુણોત્તર.
(4) ની કિંમત V O2 \u003d 7.5 અને V C6H6 \u003d 1 માં બદલી, આપણે મેળવીએ છીએ:
4. દીઠ 1 Kmole બળતણની હવાની વધુ માત્રા અભિવ્યક્તિ દ્વારા નક્કી કરવામાં આવે છે:
બેન્ઝિન વરાળ દહન હવા
આ અભિવ્યક્તિના મૂલ્યોની અવેજી
37,7(0,2-1)=30,16(7)
5. બળતણ પદાર્થની એકમ રકમ દીઠ દહન ઉત્પાદનોની કુલ રકમ રકમ દ્વારા નક્કી કરવામાં આવે છે:
મૂલ્યોના અવેજી પછી અને આપણે મેળવીએ છીએ:
6. દહન ઉત્પાદનોના દાolaના અપૂર્ણાંક, જે ટકાવારી તરીકે વ્યક્ત કરવામાં આવે છે, તે નીચે મુજબ નક્કી કરવામાં આવે છે:
કમ્બશન પ્રોડક્ટ્સમાં નાઇટ્રોજન અને ઓક્સિજનના દાola અપૂર્ણાંક માટેના સૂત્રો (9) માં હવામાં આ પદાર્થોના દાolaી અપૂર્ણાંક છે, જેનો વધુ ભાગ નાઇટ્રોજનના અપૂર્ણાંકમાં વધારો અને દહન ઉત્પાદનોમાં ઓક્સિજનના દેખાવ તરફ દોરી જાય છે.
7. ચોક્કસ વોલ્યુમો અને કમ્બશન ઉત્પાદનો નક્કી કરવા માટે, તેમના દા mની માત્રાની ગણતરી કરવી જરૂરી છે - એક કિલોમોલ ગેસનું વોલ્યુમ તે સ્થિતિમાં જેમાં ઉત્પાદનો સ્થિત છે:
જ્યાં 22.4 એ સામાન્ય સ્થિતિમાં એક કિલોગ્રામ ગેસનું પ્રમાણ છે, ટી 0 \u003d 273K એ સામાન્ય તાપમાન છે, પો \u003d 101325Pa એ સામાન્ય દબાણ છે.
(10) ની કિંમતો, પો, ટુ, માં મેળવીએ છીએ:
ઉત્પાદનોની માત્રા કે જે એક કિલોગ્રામ બળતણના દહન દરમિયાન રચાય છે, વધારાની હવાને બાદ કરતા, નીચેની ગણતરી કરવામાં આવે છે:
ઇંધણનો દાળનો માસ ક્યાં છે - એક કિલોમોલ બેન્ઝિનનો સમૂહ, કિલોગ્રામમાં વ્યક્ત થાય છે. બેન્ઝીનના દાolaના સમૂહ સૂત્ર દ્વારા જોવા મળે છે:
જ્યાં એસી અને એન કાર્બનનું અણુ વજન (12) અને હાઇડ્રોજન (1), એન સી અને એન એન બેંઝિન (સી 6 એચ 6) પરમાણુમાં કાર્બન અણુ (6) અને હાઇડ્રોજન (6) ની સંખ્યા છે.
મૂલ્યોને બદલીને અને (12) માં આપણે મેળવીએ છીએ
1 કિલોગ્રામ બળતણ દીઠ વધારાનું હવાનું પ્રમાણ નીચે મુજબ નક્કી કરવામાં આવે છે:
એક કિલોમોલ અતિરિક્ત હવાનું પ્રમાણ ક્યાં છે, જે દહન ઉત્પાદનોની રચનામાં છે. વધુ પડતા હવાનું તાપમાન અને દબાણ દહન ઉત્પાદનોના તાપમાન અને દબાણને અનુરૂપ હોવાથી, \u003d \u003d 220.7.
આ મૂલ્યની સાથે સાથે (14) માં, અમને મળે છે:
બળતણના સંપૂર્ણ કમ્બશનનાં ઉત્પાદનોના ચોક્કસ વોલ્યુમની ગણતરી કરવા માટે, અમે માની લઈશું કે બેન્ઝિન વરાળના દબાણ પર તાપમાન ટી.જી.
તાપમાન ટી.જી. અને પ્રેશર પર એક કિલોમોલ બેન્ઝિન વરાળનું પ્રમાણ ક્યાં છે? બળતણનું દાola વોલ્યુમ સૂત્ર દ્વારા ગણવામાં આવે છે:
(17) માં પ્રાપ્ત કરેલ મૂલ્ય અને આવા મૂલ્યોની જગ્યાએ, અમને મળે છે:
બેન્ઝિન વરાળના એક ઘનમીટર દીઠ વધારાનું હવાનું પ્રમાણ નીચે મુજબ નક્કી કરવામાં આવે છે:
(20) મૂલ્યો \u003d 30.16, \u003d અને માં અવેજી
નીચે આપેલ આઉટપુટ આપે છે:
વધારાની હવાને ધ્યાનમાં લેતા દહન ઉત્પાદનોનો કુલ વિશિષ્ટ વોલ્યુમ, સરવાળો દ્વારા નક્કી કરવામાં આવે છે
ગણતરી પરિણામ:
એક્સ સીઓ 2 \u003d%; એક્સ એચ 2 ઓ \u003d 4.4%; એક્સ એન 2 \u003d%; X O2 \u003d 11.7%
સમાન દસ્તાવેજો
નાઇટ્રોબેન્ઝિન Н6Н5NО2 અને કાર્બન ડિસલ્ફાઇડ સીએસ 2 ના જ્વલનશીલતા ગુણાંકની ગણતરી. હવામાં પ્રોપાયલ એસિટેટના કમ્બશન માટે પ્રતિક્રિયા સમીકરણ. જ્વલનશીલ ગેસના કમ્બશન દરમિયાન હવાના જથ્થા અને દહન ઉત્પાદનોની ગણતરી. વી. બ્લિનોવના સૂત્ર અનુસાર ટોલ્યુએનના ફ્લેશ પોઇન્ટનું નિર્ધારણ.
પરીક્ષણ, 04/08/2017 ઉમેર્યું
પદાર્થના દહન દરમિયાન રચિત હવા અને દહન ઉત્પાદનોની માત્રાની ગણતરી. હવામાં ઇથિલિન ગ્લાયકોલના કમ્બશન માટે પ્રતિક્રિયા સમીકરણ. જ્વલનશીલ વાયુઓના મિશ્રણનું દહન. સ્ટichચિઓમેટ્રિક મિશ્રણ માટે એડિએબેટિક કમ્બશન તાપમાનની ગણતરી. પ્રોપેનોલનું દહન.
પરીક્ષણ, 10/17/2012 ઉમેર્યું
દહન પ્રકાર અને તેના મુખ્ય પરિમાણો. બળતણ અને ઓક્સિડાઇઝરનું રાસાયણિક રૂપાંતર દહન ઉત્પાદનોમાં. દહન પ્રતિક્રિયાના સામગ્રી અને ગરમી સંતુલનના સમીકરણો. કમ્બશન ઉત્પાદનો અને કમ્બશન તાપમાનની રચના પર વધતા હવાના પ્રમાણનો પ્રભાવ.
પરીક્ષણ, 01/17/2013 ઉમેર્યું
જ્વલનશીલ પદાર્થના એકમ માસના સંપૂર્ણ દહન માટે જરૂરી હવાના જથ્થાનું નિર્ધારણ. જ્વલનશીલ પદાર્થના એકમ માસના દહન ઉત્પાદનોની રચના. ગેસ, વરાળ, ધૂળ-હવા મિશ્રણની જ્યોત ફેલાવાની મર્યાદા. વિસ્ફોટક વિઘટન દબાણ.
ટર્મ પેપર, 12/23/2013 ઉમેર્યું
આગ અને વિસ્ફોટોની ઘટનાને રોકવા માટેના પગલાઓનો વિકાસ, તેમના વિકાસ અને દમન માટેની પરિસ્થિતિઓની આકારણી. બર્નઆઉટ રેટની વિભાવના, તેને નિર્ધારિત કરવાની રીત. દહન પ્રતિક્રિયાના સમીકરણને દોરવાની પ્રક્રિયા. ઇગ્નીશન માટે જરૂરી હવાના જથ્થાની ગણતરી.
ટર્મ પેપર, 07/10/2014 ઉમેર્યું
સંપૂર્ણ ગેસ કમ્બશનના ઉત્પાદનોની રચનાનું નિર્ધારણ. સતત વોલ્યુમ અને સતત દબાણમાં ગેસ મિશ્રણના દહનના એડિબેટિક તાપમાનની ગણતરી. કુદરતી ગેસની સ્વચાલિત પ્રતિક્રિયાના ગતિશીલ સ્થિરતા. ગેસ મિશ્રણની જ્વલનશીલતા મર્યાદા.
ટર્મ પેપર 02/19/2014 ઉમેર્યું
પ્રોપિલિન સાથે બેન્ઝિનના આલ્કિલેશન માટે industrialદ્યોગિક પદ્ધતિઓનું લક્ષણ. રાસાયણિક તકનીકમાં ઓલેફિન્સ સાથે બેન્ઝિન એલ્કલેશનના સિદ્ધાંતો. બેન્ઝિન એલ્કેલેશન માટે તકનીકી એકમોની રચના કરવામાં સમસ્યા. ઉત્પાદન પ્રક્રિયાની તકનીકીનું વર્ણન.
થીસીસ, 11/15/2010 ઉમેર્યું
શક્તિશાળી ઓક્સિડેશન પ્રક્રિયા તરીકે દહન. દહન પ્રકાર: ધૂમ્રપાન અને જ્યોત સાથે બર્ન. દહનના વિશેષ કેસ તરીકે વિસ્ફોટ. જ્યોત વિદ્યુત ગુણધર્મો. બળતણના અપૂર્ણ દહનના પરિણામે દહન ઉત્પાદનોની વિવિધતા. પાણી દ્વારા ધુમાડો ગાળવું.
વૈજ્ scientificાનિક કાર્ય, 07/29/2009 ઉમેર્યું
પ્રોપેનની આપેલ રકમના સંપૂર્ણ દહન માટે જરૂરી હવાના પ્રમાણનું નિર્ધારણ. હેસના કાયદાના પરિણામોનો ઉપયોગ કરીને એન્થેલ્પી, એન્ટ્રોપી અને ગિબ્સ energyર્જામાં પરિવર્તનની ગણતરી. ઓક્સિડાઇઝિંગ એજન્ટ અને ઘટાડેલા એજન્ટની સમકક્ષની દાળની જનતાનું નિર્ધારણ.
પરીક્ષણ, 02/08/2012 ઉમેર્યું
શોષણ તેલના વપરાશને નિર્ધારિત કરવાની પદ્ધતિઓ, શોષક તેલમાં બેન્ઝિનની સાંદ્રતા શોષકને છોડે છે. પેક્ડ શોષકના વ્યાસ અને .ંચાઈની ગણતરી. સ્તંભના સમઘન અને હીટિંગ વરાળ વપરાશની આવશ્યક ગરમીની સપાટીનું નિર્ધારણ.
સુગંધિત એચસી (એરેનાસ) હાઇડ્રોકાર્બન છે, તે પરમાણુઓ એક અથવા વધુ બેન્ઝિન રિંગ્સ ધરાવે છે.
સુગંધિત હાઇડ્રોકાર્બનનાં ઉદાહરણો:

બેન્ઝિન શ્રેણી એરેનાસ (મોનોસાયક્લિક એરેનાસ)
સામાન્ય સૂત્ર:સી એન એચ 2 એન -6, એન-6
સુગંધિત હાઇડ્રોકાર્બનનો સૌથી સરળ પ્રતિનિધિ બેંઝિન છે, તેનું પ્રયોગમૂલક સૂત્ર С 6 Н 6 છે.
બેન્ઝીન પરમાણુની ઇલેક્ટ્રોનિક રચના
મોનોસાયક્લિક એરેન્સ સી એન એચ 2 એન -6 નો સામાન્ય સૂત્ર સૂચવે છે કે તેઓ અસંતૃપ્ત સંયોજનો છે.
1856 માં જર્મન રસાયણશાસ્ત્રી એ.એફ. કેકુલેએ કન્ઝ્યુગેટેડ બોન્ડ્સ (વૈકલ્પિક સિંગલ અને ડબલ બોન્ડ્સ) - સાયક્લોહેક્સેટ્રિએન-1,3,5 સાથે બેન્ઝિનનું ચક્રીય સૂત્ર પ્રસ્તાવિત કર્યું: 
બેન્ઝીન પરમાણુની આ રચનામાં બેન્ઝીનના ઘણા ગુણધર્મો સમજાવ્યા નથી:
- બેન્ઝિન માટે, અવેજી પ્રતિક્રિયાઓ લાક્ષણિકતા છે, અને અસંતૃપ્ત સંયોજનોની વિશિષ્ટતાની પ્રતિક્રિયા નથી. વધારાની પ્રતિક્રિયાઓ શક્ય છે, પરંતુ તેના કરતા વધુ મુશ્કેલ છે;
- બેન્ઝિન પ્રતિક્રિયાઓમાં પ્રવેશ કરતી નથી જે અસંતૃપ્ત હાઇડ્રોકાર્બન (બ્રોમિન પાણી અને KMnO 4 ના સોલ્યુશન સાથે) માટે ગુણાત્મક પ્રતિક્રિયાઓ છે.
પાછળથી હાથ ધરવામાં આવેલા ઇલેક્ટ્રોન વિખેરણ અધ્યયનોએ દર્શાવ્યું કે બેન્ઝિન પરમાણુમાં કાર્બન અણુઓ વચ્ચેના બધા બંધનોની લંબાઈ 0.140 એનએમ જેટલી હોય છે (એક જ સી-સી બોન્ડની લંબાઈ વચ્ચે સરેરાશ મૂલ્ય 0.154 એનએમ અને ડબલ બોન્ડ સી \u003d સી 0.134 એનએમ છે). દરેક કાર્બન અણુ માટેના બોન્ડ્સ વચ્ચેનું કોણ 120 ° છે. પરમાણુ નિયમિતપણે ફ્લેટ ષટ્કોણ છે.
સી 6 એચ 6 પરમાણુની રચનાને સમજાવવા માટેનો આધુનિક સિધ્ધાંતણુ અણુની ભ્રમણકક્ષાના વર્ણસંકરકરણની વિભાવનાનો ઉપયોગ કરે છે.
બેન્ઝીનમાં કાર્બન અણુ એસપી 2-હાઇબ્રીડિએશનની સ્થિતિમાં છે. દરેક "સી" અણુ ત્રણ three-બોન્ડ બનાવે છે (કાર્બન અણુ સાથે બે અને હાઇડ્રોજન અણુ સાથે એક). બધા σ-બોન્ડ્સ સમાન પ્લેનમાં છે:
દરેક કાર્બન અણુમાં એક પી-ઇલેક્ટ્રોન હોય છે, જે સંકરમાં ભાગ લેતો નથી. કાર્બન અણુઓની પીં-ઓર્બિટલ્સ કાર્બન પરમાણુ σ-બોન્ડ્સના વિમાનની કાટખૂણે હોય છે. દરેક પી-ક્લાઉડ બે પડોશી પી-વાદળોથી overવરલેપ થાય છે, અને પરિણામે, એક જ સંયુક્ત π-સિસ્ટમ રચાય છે ("ડાયેન હાઇડ્રોકાર્બન" વિષયમાં ચર્ચા કરેલા 1,3-બટadiડિઅન પરમાણુમાં પી-ઇલેક્ટ્રોનની અસરને યાદ કરો):
એક જ સિસ્ટમ સાથે છ σ-બોન્ડ્સનું સંયોજન કહેવામાં આવે છે સુગંધિત બંધન.
સુગંધિત બંધન દ્વારા જોડાયેલા છ કાર્બન અણુઓનું એક ચક્ર કહેવામાં આવે છે બેન્ઝિન રિંગઅથવા બેન્ઝિન બીજક.
બેન્ઝિનની ઇલેક્ટ્રોનિક રચના વિશેના આધુનિક વિચારો અનુસાર, સી 6 એચ 6 પરમાણુ નીચે મુજબ નિરૂપણ કરવામાં આવ્યું છે:

બેન્ઝીનની શારીરિક ગુણધર્મો
સામાન્ય સ્થિતિમાં બેંઝિન એ રંગહીન પ્રવાહી છે; t o pl \u003d 5.5 સે વિશે; ટી ઓ બેલ. \u003d 80 સે વિશે; એક લાક્ષણિકતા ગંધ છે; પાણીથી ભેળસેળ કરવા યોગ્ય નહીં, સારા દ્રાવક, ખૂબ ઝેરી.
બેન્ઝીનની રાસાયણિક ગુણધર્મો
સુગંધિત બંધન બેન્ઝીન અને અન્ય સુગંધિત હાઇડ્રોકાર્બનના રાસાયણિક ગુણધર્મો નક્કી કરે છે.
પરંપરાગત બે ઇલેક્ટ્રોન b-બોન્ડ્સ કરતાં 6π-ઇલેક્ટ્રોન સિસ્ટમ વધુ સ્થિર છે. તેથી, સુગંધિત હાઇડ્રોકાર્બન માટે અસંતૃપ્ત હાઇડ્રોકાર્બન કરતાં વધારાની પ્રતિક્રિયાઓ ઓછી લાક્ષણિક છે. બદલીની પ્રતિક્રિયા એરેન્સ માટે સૌથી લાક્ષણિક છે.
હું... બદલી પ્રતિક્રિયાઓ
1. હેલોજેનેશન

2. નાઈટ્રેશન
પ્રતિક્રિયા એસિડ્સ (નાઇટ્રેટિંગ મિશ્રણ) ના મિશ્રણ સાથે કરવામાં આવે છે: 
S.સૂફ્નેશન

4. અલકીલેશન (અલ્કિલ જૂથ માટે "એચ" અણુનો અવેજી) - ફ્રિડેલ-હસ્તકલાની પ્રતિક્રિયાઓ, બેન્ઝિન હોમોલોગ્સ રચાય છે:

હેલોકનેકસને બદલે, એલ્કેન્સનો ઉપયોગ કરી શકાય છે (ઉત્પ્રેરકની હાજરીમાં - અલસીએલ 3 અથવા અકાર્બનિક એસિડ):

II... વધારાની પ્રતિક્રિયાઓ
1. હાઇડ્રોજન

2. કલોરિનનું એડિશન

III. ઓક્સિડેશન પ્રતિક્રિયાઓ
1. દહન
2С 6 Н 6 + 15О 2 → 12СО 2 + 6Н 2 О
2. અપૂર્ણ ઓક્સિડેશન (એસિડિક વાતાવરણમાં KMnO 4 અથવા K 2 Cr 2 O 7). બેંઝિન રિંગ oxક્સિડાઇઝિંગ એજન્ટો માટે પ્રતિરોધક છે. કોઈ પ્રતિક્રિયા થતી નથી.
બેન્ઝીન મેળવવું
ઉદ્યોગમાં:
1) તેલ અને કોલસાની પ્રક્રિયા;
2) સાયક્લોહેક્ઝેનનું ડિહાઇડ્રોજનરેશન:

)) ષટ્કોણનું ડિહાઇડ્રોસાયક્લાઈઝેશન (સુગંધિત):

પ્રયોગશાળામાં:
આ સાથે બેન્ઝોઇક એસિડના મીઠાનું મિશ્રણ:

આઇસોમેરિઝમ અને બેન્ઝિન હોમોલોગ્સનું નામકરણ
કોઈપણ બેન્ઝિન હોમોલોગમાં સાઇડ ચેન હોય છે, એટલે કે. બેન્ઝિન રિંગ સાથે જોડાયેલ એલ્કિલ રેડિકલ્સ. પ્રથમ બેન્ઝિન હોમોલોગ એ બેંઝિન રિંગ છે જે મિથાઇલ આમૂલ સાથે જોડાયેલી છે: 
ટોલુએન પાસે કોઈ આઇસોમર્સ નથી, કારણ કે બેન્ઝિન રીંગમાંની બધી સ્થિતિઓ સમાન છે.
બેન્ઝિનના અનુગામી હોમોલોગ્સ માટે, એક પ્રકારનું આઇસોમેરિઝમ શક્ય છે - સાઇડ ચેઇનનો આઇસોમેરિઝમ, જે બે પ્રકારના હોઈ શકે છે:
1) અવેજીઓની સંખ્યા અને બંધારણનો આઇસોમેરિઝમ;
2) અવેજીઓની સ્થિતિનું આઇસોમેરિઝમ.



ટોલ્યુએનની શારીરિક ગુણધર્મો
ટોલુએન - લાક્ષણિકતા ગંધવાળી રંગહીન પ્રવાહી, પાણીમાં અદ્રાવ્ય, કાર્બનિક દ્રાવકોમાં સારી રીતે દ્રાવ્ય. બેનઝિન કરતા ટોલુએન ઓછું ઝેરી છે.
ટોલ્યુએનનું રાસાયણિક ગુણધર્મો
હું... બદલી પ્રતિક્રિયાઓ
1. બેન્ઝિન રિંગને લગતી પ્રતિક્રિયાઓ
મેથિલબેન્ઝિન તે તમામ અવેજી પ્રતિક્રિયાઓમાં પ્રવેશ કરે છે જેમાં બેન્ઝિન ભાગ લે છે, અને ઉચ્ચ પ્રતિક્રિયા દર્શાવે છે, પ્રતિક્રિયાઓ higherંચા દરે આગળ વધે છે.
ટોલ્યુએન પરમાણુમાં રહેલ મિથાઈલ ર radડિકલ એ જીનસનો અવેજી છે, તેથી, બેંઝિન રિંગમાં ઓર્થો- અને પેરા-ડેરિવેટિવ્ઝ મેળવવામાં આવે છે અથવા, સામાન્ય સૂત્રના ત્રણેય વ્યુત્પત્તિઓ સાથે, રેગ્યુએન્ટના વધુ સાથે:

એ) હેલોજેનેશન


વધુ ક્લોરીનેશન સાથે, ડિક્લોરોમિથિલબેન્ઝિન અને ટ્રાઇક્લોરોમિથાઇલબેન્ઝિન મેળવી શકાય છે:

II... વધારાની પ્રતિક્રિયાઓ
હાઇડ્રોજન

III.ઓક્સિડેશન પ્રતિક્રિયાઓ
1. બર્નિંગ
સી 6 એચ 5 સીએચ 3 + 9 ઓ 2 → 7 સી 2 + 4 એચ 2 ઓ
2. અપૂર્ણ ઓક્સિડેશન
બેન્ઝિનથી વિપરીત, તેના હોમોલોગ્સ કેટલાક ઓક્સિડાઇઝિંગ એજન્ટો દ્વારા ઓક્સિડાઇઝ્ડ કરવામાં આવે છે; આ કિસ્સામાં, બાજુની સાંકળ ઓક્સિડેશનમાંથી પસાર થાય છે, મિથિલ જૂથ ટોલ્યુએનના કિસ્સામાં. હળવા ઓક્સિડાઇઝિંગ એજન્ટો જેમ કે MnO 2 તેને ઓલ્ડીહાઇડ જૂથમાં ઓક્સિડાઇઝ કરે છે, મજબૂત ઓક્સિડેન્ટ્સ (KMnO 4) એસિડમાં વધુ ઓક્સિડેશનનું કારણ બને છે: 
એક બાજુ સાંકળવાળા બેન્ઝિનના કોઈપણ હોમોલોગને કે.એમ.એન.ઓ. 4 થી બેન્ઝોઇક એસિડ જેવા મજબૂત ઓક્સિડાઇઝિંગ એજન્ટ દ્વારા ઓક્સિડાઇઝ કરવામાં આવે છે, એટલે કે. બાજુના સાંકળના ભાગને વિભાજનના offક્સિડેશન સાથે તોડીને СО 2; દા.ત. 
જો ઘણી બાજુ સાંકળો હોય, તો તેમાંથી દરેકને કાર્બોક્સિલ જૂથમાં ઓક્સિડાઇઝ કરવામાં આવે છે અને પરિણામે, પોલિબેસિક એસિડ્સ રચાય છે, ઉદાહરણ તરીકે:

Toluene ઉત્પાદન:
ઉદ્યોગમાં:
1) તેલ અને કોલસાની પ્રક્રિયા;
2) મેથિલસિક્લોહેક્ઝેનનું ડિહાઇડ્રોજનરેશન:

3) હેપ્ટેનનું ડિહાઇડ્રોસાયક્લાઇઝેશન:
પ્રયોગશાળામાં:
1) ફ્રિડેલ-હસ્તકલા એલ્કલેશન;
2) વોર્ઝ-ફીટિગ પ્રતિક્રિયા (હેલોજેનબેનેઝિન અને હloલોકેનના મિશ્રણ સાથે સોડિયમની ક્રિયાપ્રતિક્રિયા).
એરેનાસ (સુગંધિત હાઇડ્રોકાર્બન) – આ અસંતૃપ્ત (અસંતૃપ્ત) ચક્રીય હાઇડ્રોકાર્બન છે, તેમાં પરમાણુઓના સ્થિર ચક્રીય જૂથો (બેન્ઝિન ન્યુક્લી) સમાયેલ બોન્ડ્સની બંધ સિસ્ટમ સાથે સમાયેલ છે.
સામાન્ય સૂત્ર: સી એન એચ 2 એન - 6એન ≥ 6 માટે.
એરેન્સના રાસાયણિક ગુણધર્મો
એરેનાસ- અસંતૃપ્ત હાઇડ્રોકાર્બન, તે પરમાણુઓ જેમાં ત્રણ ડબલ બોન્ડ અને એક ચક્ર હોય છે. પરંતુ જોડાણની અસરને લીધે, એનેસની ગુણધર્મો અન્ય અસંતૃપ્ત હાઇડ્રોકાર્બન કરતા અલગ પડે છે.
સુગંધિત હાઇડ્રોકાર્બન પ્રતિક્રિયાઓ દ્વારા વર્ગીકૃત થયેલ છે:
- પ્રવેશ
- અવેજી,
- ઓક્સિડેશન (બેન્ઝિન હોમોલોગ્સ માટે).
બેન્ઝિનની સુગંધિત સિસ્ટમ oxક્સિડેન્ટ્સ માટે પ્રતિરોધક છે. જો કે, બેન્ઝિન હોમોલોગ્સ પોટેશિયમ પરમેંગેનેટ અને અન્ય oxક્સિડાઇઝિંગ એજન્ટો દ્વારા oxક્સિડાઇઝ્ડ કરવામાં આવે છે.
1. ઉમેરો પ્રતિક્રિયાઓ
બzન્ઝિન જ્યારે ઉત્પ્રેરકની હાજરીમાં ગરમ \u200b\u200bથાય છે ત્યારે પ્રકાશ અને હાઇડ્રોજનમાં કલોરિન ઉમેરે છે.
1.1. હાઇડ્રોજન
મેટલ ઉત્પ્રેરક (ની, પીટી, વગેરે) ની હાજરીમાં જ્યારે ગરમ થાય છે અને દબાણમાં આવે છે ત્યારે બેન્ઝિન હાઇડ્રોજન ઉમેરે છે.
જ્યારે બેન્ઝીન હાઇડ્રોજનયુક્ત હોય છે, ત્યારે સાયક્લોહેક્સાઇન રચાય છે:
હોમોલોગ્સના હાઇડ્રોજનને આધારે સાયક્લોલકેન ડેરિવેટિવ્ઝની રચના થાય છે. જ્યારે દબાણમાં હાઈડ્રોજનથી અને ઉત્પ્રેરકની હાજરીમાં ટોલ્યુએન ગરમ થાય છે, ત્યારે મેથાઈલસાયક્લોહેક્સાન્સ રચાય છે:
૧. 1.2. એરેનાઝનું ક્લોરીનેશન
બેંઝિનમાં કલોરિનનો ઉમેરો આગળ વધે છે ઉંચા તાપમાને આમૂલ મિકેનિઝમ દ્વારા, અલ્ટ્રાવાયોલેટ કિરણોત્સર્ગના પ્રભાવ હેઠળ.
જ્યારે બેન્ઝીન પ્રકાશમાં કલોરિનેટેડ હોય છે, 1,2,3,4,5,6-hexachlorocyclohexane (hexachloran).
હેક્સાચ્લોરન એ એક જંતુનાશક છે જેનો ઉપયોગ હાનિકારક જંતુઓને નિયંત્રણમાં કરવા માટે થાય છે. હાલમાં હેક્સાક્લોરેનનો ઉપયોગ પ્રતિબંધિત છે.
બેન્ઝીનના હોમોલોગ્સ કલોરિન ઉમેરતા નથી. જો બેન્ઝિન હોમોલોગ કલોરિન અથવા બ્રોમિન સાથે પ્રતિક્રિયા આપે છે પ્રકાશ અથવા highંચા તાપમાને (300 ° સે), પછી હાઇડ્રોજન અણુની ફેરબદલ થાય છે સુગંધિત રિંગને બદલે પેન્ડન્ટ એલ્કિલ અવેજીમાં.
2. બદલી પ્રતિક્રિયાઓ
2.1. હેલોજેનેશન
બેન્ઝિન અને તેના હોમોલોગ્સ ઉત્પ્રેરકની હાજરીમાં હેલોજેન્સ (કલોરિન, બ્રોમિન) સાથે અવેજી પ્રતિક્રિયાઓ દાખલ કરે છે (એએલસીએલ 3, ફેબીઆર 3) .
જ્યારે ઉત્પ્રેરક AlCl 3 પર કલોરિન સાથે વાતચીત થાય છે, ત્યારે ક્લોરોબેન્ઝિનની રચના થાય છે:
સુગંધિત હાઇડ્રોકાર્બન ગરમ થાય ત્યારે બ્રોમિન સાથે સંપર્ક કરે છે અને ઉત્પ્રેરકની હાજરીમાં - ફેબીઆર 3. ઉપરાંત, ધાતુ આયર્નનો ઉપયોગ ઉત્પ્રેરક તરીકે થઈ શકે છે.
બ્રોમાઇન લોખંડ સાથે પ્રતિક્રિયા આપે છે આયર્ન (III) બ્રોમાઇડ બનાવે છે, જે બેન્ઝીનની બ્રોમિનેશનને ઉત્પ્રેરિત કરે છે:
મેટાch-chlorotoluene ઓછી માત્રામાં રચાય છે.
બેન્ઝીન હોમોલોગ્સની ક્રિયાપ્રતિક્રિયામાં પ્રકાશ અથવા temperaturesંચા તાપમાને હેલોજેન્સ સાથે (300 о С) હાઇડ્રોજન બેન્જિન રિંગમાં નહીં, પરંતુ સાઇડ હાઇડ્રોકાર્બન રેડિકલમાં બદલાઈ જાય છે.
ઉદાહરણ તરીકે, જ્યારે ક્લોરીનેટિંગ ઇથિલબેન્ઝિન:
2.2. નાઈટ્રેશન
બેન્ઝેન, કોન્સેન્ટ્રેટેડ સલ્ફ્યુરિક એસિડ (નાઇટ્રેટિંગ મિશ્રણ) ની હાજરીમાં કેન્દ્રિત નાઇટ્રિક એસિડ સાથે પ્રતિક્રિયા આપે છે.
આ નાઇટ્રોબેન્ઝિન બનાવે છે:
ટોલ્યુએન, કોન્સેન્ટ્રેટેડ સલ્ફ્યુરિક એસિડની હાજરીમાં કેન્દ્રિત નાઇટ્રિક એસિડ સાથે પ્રતિક્રિયા આપે છે.
પ્રતિક્રિયાવાળા ઉત્પાદનોમાં, અમે ક્યાં સૂચવે છે વિશે-નિત્રોટોલીયુએન:
અથવા પી-નિત્રોટોલીયુએન:
ત્રણ હાઇડ્રોજન અણુના અવેજી સાથે પણ ટોલ્યુએન નાઈટ્રેશન આગળ વધી શકે છે. આ 2,4,6-trinitrotoluene (TNT, tol) ઉત્પન્ન કરે છે:
૨.3. સુગંધિત હાઇડ્રોકાર્બનનું એલેક્લેશન
- બેન્ઝિન હોમોલોગ રચવા માટે એરેન્સ ઉત્પ્રેરકની હાજરીમાં (એએલસીએલ 3, ફેબીઆર 3, વગેરે) હ haલોકનેઝ સાથે સંપર્ક કરે છે.
- સુગંધિત હાઇડ્રોકાર્બન એલ્યુમિનિયમ ક્લોરાઇડ, આયર્ન (III) બ્રોમાઇડ, ફોસ્ફોરિક એસિડ, વગેરેની હાજરીમાં અલકેન્સ સાથે સંપર્ક કરે છે.
- આલ્કોહોલ સાથેની આલ્કિલેશન, કેન્દ્રિત સલ્ફ્યુરિક એસિડની હાજરીમાં થાય છે.
2.4. સુગંધિત હાઇડ્રોકાર્બનનું સલ્ફોનેશન
બેન્ઝેન પ્રતિક્રિયા આપે છે જ્યારે કોન્સેન્ટ્રેટેડ સલ્ફ્યુરિક એસિડથી ગરમ થાય છે અથવા સલ્ફ્યુરિક એસિડ (ઓલિયમ) માં એસઓ 3 ના સોલ્યુશનથી બેન્ઝેનેસલ્ફોનિક એસિડ રચાય છે:
3. અખાડોનું ઓક્સિડેશન
બેંઝિન પણ મજબૂત ઓક્સિડેન્ટની ક્રિયા સામે પ્રતિરોધક છે. પરંતુ બેન્ઝિનના હોમોલોગ્સ મજબૂત ઓક્સિડેન્ટ્સ દ્વારા oxક્સિડાઇઝ્ડ કરવામાં આવે છે. બેન્ઝિન અને તેના હોમોલોગ્સ સળગી રહ્યા છે.
3.1. સંપૂર્ણ ઓક્સિડેશન - કમ્બશન
જ્યારે બેન્ઝીન અને તેના હોમોલોગ્સ બર્ન થાય છે, ત્યારે કાર્બન ડાયોક્સાઇડ અને પાણી રચાય છે. એરેન્સની કમ્બશન પ્રતિક્રિયા એ મોટી માત્રામાં ગરમીના પ્રકાશન સાથે છે.
2 સી 6 એચ 6 + 15 ઓ 2 → 12 સીઓ 2 + 6 એચ 2 ઓ + ક્યૂ
એરેન કમ્બશન સમીકરણનું સામાન્ય સ્વરૂપ:
સી એન એચ 2 એન - 6 + (3 એન - 3) / 2 ઓ 2 → એનકો 2 + (એન - 3) એચ 2 ઓ + પ્ર
જ્યારે ઓક્સિજનના અભાવમાં સુગંધિત હાઇડ્રોકાર્બન બળી જાય છે, ત્યારે કાર્બન મોનોક્સાઇડ સીઓ અથવા સૂટ સીની રચના થઈ શકે છે.
બેન્ઝિન અને તેના હોમોલોગ ધૂમ્રપાનની જ્યોતથી હવામાં બળીને જાય છે. બેન્ઝિન અને તેના હોમોલોગ્સ હવા અને ઓક્સિજન સાથે વિસ્ફોટક મિશ્રણ બનાવે છે.
2.૨. વિશેબેન્ઝીન હોમોલોગ્સનું એસિડિફિકેશન
બેન્ઝિનના હોમોલોગ્સ એસિડિક અથવા તટસ્થ માધ્યમમાં હીટિંગ પછી પરમેંગેનેટ અને પોટેશિયમ ડાયક્રોમેટ દ્વારા સહેલાઇથી ઓક્સિડાઇઝ્ડ કરવામાં આવે છે.
જ્યારે આવું થાય છે કાર્બન અણુ પરના તમામ બોન્ડનું oxક્સિડેશનબેન્ઝિન રિંગની બાજુમાં, બેન્ઝિન રીંગ સાથેના આ કાર્બન અણુના બંધન સિવાય.
ટોલ્યુએન ઓક્સિડાઇઝ્ડ છે સલ્ફરિક એસિડમાં પોટેશિયમ પરમેંગેનેટ શિક્ષણ સાથે બેન્ઝોઇક એસિડ:
જો ટોલ્યુએન ઓક્સિડાઇઝ્ડ છે તટસ્થ ઉકેલમાં જ્યારે ગરમ થાય છે, પછી બેન્ઝોઇક એસિડ મીઠું - પોટેશિયમ બેન્ઝોએટ:
આમ, ટોલ્યુએન એસિડિફાઇડ પોટેશિયમ પરમેંગેનેટ સોલ્યુશનને ડીકોલોરાઇઝ કરે છે જ્યારે ગરમ.
લાંબી ર radડિકલ્સ બેંઝોઇક એસિડ અને કાર્બોક્સિલિક એસિડમાં ઓક્સિડાઇઝ્ડ હોય છે:
જ્યારે પ્રોપિલબેન્ઝિન ઓક્સિડાઇઝ્ડ થાય છે, ત્યારે બેન્ઝોઇક અને એસિટિક એસિડ્સ બને છે:
ઇસોપ્રોપીલબેન્ઝિન એ એસિડિક માધ્યમમાં પોટેશિયમ પરમેંગેનેટ દ્વારા બેંઝોઇક એસિડ અને કાર્બન ડાયોક્સાઇડમાં ઓક્સિડાઇઝ્ડ કરવામાં આવે છે:
4. બેન્ઝિન રિંગમાં અવેજીઓની દિશાલક્ષી અસર
જો બેન્ઝિન રિંગમાં અર્કિલ જ નહીં, પરંતુ અન્ય અણુઓ (હાઇડ્રોક્સિલ, એમિનો જૂથ, નાઇટ્રો જૂથ, વગેરે) પણ હોય છે, તો સુગંધિત પ્રણાલીમાં હાઇડ્રોજન અણુની ફેરબદલની પ્રતિક્રિયાઓ, પ્રકૃતિ અનુસાર, સખત રીતે વ્યાખ્યાયિત રીતે આગળ વધે છે. સુગંધિત system-સિસ્ટમ પર અવેજીનો પ્રભાવ.
બેન્ઝીન રિંગ પર અવેજીના પ્રકારો
| પ્રથમ પ્રકારના નાયબ | બીજા પ્રકારનાં અવેજી |
| ઓર્થો- અને દંપતી-પોઝિશન | વધુ અવેજી મુખ્યત્વે થાય છે મેટા-પોઝિશન |
| ઇલેક્ટ્રોન દાતા, બેન્ઝિન રિંગમાં ઇલેક્ટ્રોનની ઘનતા વધારવી | ઇલેક્ટ્રોન-સ્વીકારનાર, સંયુક્ત પ્રણાલીમાં ઇલેક્ટ્રોન ઘનતા ઘટાડે છે. |
|
|
શારીરિક ગુણધર્મો
બેન્ઝિન અને તેના નજીકના હોમોલોગ્સ ચોક્કસ ગંધવાળા રંગહીન પ્રવાહી છે. સુગંધિત હાઇડ્રોકાર્બન પાણી કરતા હળવા હોય છે અને તેમાં ભળી જતા નથી, પરંતુ તે સજીવ સોલવન્ટ્સ - આલ્કોહોલ, ઈથર, એસિટોનથી સરળતાથી ઓગળી જાય છે.
બેંઝિન અને તેના હોમોલોગ્સ ઘણા સજીવ પદાર્થો માટે પોતાને સારા દ્રાવક છે. બધા અખાડો તેમના પરમાણુઓમાં કાર્બનનું પ્રમાણ વધારે હોવાને કારણે તે સ્મોકી જ્યોતથી બળી જાય છે.
કેટલાક અખાડોની શારીરિક ગુણધર્મો કોષ્ટકમાં રજૂ કરવામાં આવે છે.
ટેબલ. કેટલાક અખાડોની શારીરિક ગુણધર્મો
|
નામ |
ફોર્મ્યુલા |
ટી ° .પીએલ., |
ટી °. ઉકાળો |
|
બેન્ઝિન |
સી 6 એચ 6 |
5,5 |
80,1 |
|
ટોલ્યુએન (મિથાઈલબેન્ઝિન) |
સી 6 એચ 5 સીએચ 3 |
95,0 |
110,6 |
|
એથિલબેન્ઝિન |
સી 6 એચ 5 સી 2 એચ 5 |
95,0 |
136,2 |
|
ઝિલેન (ડાઇમિથાયલબેંઝિન) |
સી 6 એચ 4 (સીએચ 3) 2 |
||
|
ઓર્થો- |
25,18 |
144,41 |
|
|
મેટા- |
47,87 |
139,10 |
|
|
દંપતી- |
13,26 |
138,35 |
|
|
પ્રોપાયલ બેન્ઝિન |
સી 6 એચ 5 (સીએચ 2) 2 સીએચ 3 |
99,0 |
159,20 |
|
ક્યુમેન (આઇસોપ્રોપીલબેન્ઝિન) |
સી 6 એચ 5 સીએચ (સીએચ 3) 2 |
96,0 |
152,39 |
|
સ્ટીરિન (વિનાઇલ બેંઝિન) |
સી 6 એચ 5 સીએચ \u003d સીએચ 2 |
30,6 |
145,2 |
બેન્ઝિન - ઓછી ઉકળતા ( ટી ગાંસડી\u003d 80.1 ° સે), રંગહીન પ્રવાહી, પાણીમાં અદ્રાવ્ય
ધ્યાન! બેન્ઝિન - ઝેર, કિડની પર કામ કરે છે, લોહીના ફોર્મ્યુલામાં ફેરફાર કરે છે (લાંબા સમય સુધી સંપર્કમાં), રંગસૂત્રોની રચનામાં વિક્ષેપ લાવી શકે છે.
મોટાભાગના સુગંધિત હાઇડ્રોકાર્બન જીવલેણ અને ઝેરી હોય છે.
એરેન્સ મેળવવી (બેન્ઝીન અને તેના હોમોલોગ્સ)
પ્રયોગશાળામાં
1. સોલિડ આલ્કલિસિસ સાથે બેન્ઝોઇક એસિડના ક્ષારનું મિશ્રણ
સી 6 એચ 5 -કોના + નાઓએચ ટીસી 6 એચ 6 + ના 2 સીઓ 3
સોડિયમ બેન્ઝોએટ
2. વોર્ઝ-ફિટિંગ પ્રતિક્રિયા: (અહીં જી હેલોજન છે)
સી 6એચ 5 -જી + 2ના + આર-જી →સી 6 એચ 5 - આર + 2 નાડી
થી 6 H 5 -Cl + 2Na + CH 3 -Cl → C 6 H 5 -CH 3 + 2NaCl
ઉદ્યોગમાં
- અપૂર્ણાંક નિસ્યંદન દ્વારા તેલ અને કોલસાથી અલગ, સુધારણા;
- કોલસો ટાર અને કોક પકાવવાની નાની ભઠ્ઠી ગેસ માંથી
1. એલ્કેન્સનું ડિહાઇડ્રોસાયક્લાઇઝેશન 6 કરતા વધારે કાર્બન અણુઓ સાથે:
સી 6 એચ 14 ટી , કેટ6 સી 6 એચ 6 + 4 એચ 2
2. એસિટિલિન ત્રિમાસિકરણ (ફક્ત બેન્ઝીન માટે) - આર. ઝેલિંસ્કી:
3 સી 2 એચ 2 600 ° સી , અધિનિયમ. કોલસો 6 સી 6 એચ 6
3. ડિહાઇડ્રોજન સાયક્લોહેક્સાને અને તેના હોમોલોગ્સ:
સોવિયત એકેડેમિશિયન નિકોલાઈ ડિમિટ્રેવિચ ઝેલિંસ્કીએ શોધી કા that્યું કે બેન્ઝિન સાયક્લોહેક્ઝેન (સાયક્લોકkanનેક્સના ડિહાઇડ્રોજનરેશન) માંથી રચાય છે
સી 6 એચ 12 ટી, કેટ6 સી 6 એચ 6 + 3 એચ 2

સી 6 એચ 11-સીએચ 3 ટી , કેટ6 સી 6 એચ 5-સીએચ 3 + 3 એચ 2
મેથાઇલ્સીક્લોહેક્સાન્થોલ્યુએન
4. બેન્ઝીનનું આલ્કિલેશન (બેન્ઝીનના હોમોલોગ્સ પ્રાપ્ત કરવા) - પી ફ્રિડેલ-હસ્તકલા.
સી 6 એચ 6 + સી 2 એચ 5 -સીએલ t, AlCl36 સે 6 એચ 5-સી 2 એચ 5 + એચસીએલ
હરિતદ્રવ્ય ઇથિલબેન્ઝિન

એરેન્સના રાસાયણિક ગુણધર્મો
હું... ઓક્સિડેશન પ્રતિક્રિયાઓ
1. દહન (સ્મોકી જ્યોત):
2સી 6 એચ 6 + 15 ઓ 2 ટી CO 12CO 2 + 6H 2 O + Q
2. સામાન્ય સ્થિતિમાં બેંઝિન બ્રોમિનના પાણી અને પોટેશિયમ પરમેંગેનેટનું જલીય દ્રાવણ વિકૃત કરતું નથી.
3. બેન્ઝીનના હોમોલોગ્સને પોટેશિયમ પરમેંગેનેટ (ડેકોલોરાઇઝ પોટેશિયમ પરમેંગેનેટ) સાથે ઓક્સિડાઇઝ કરવામાં આવે છે:
એ) એસિડિક માધ્યમથી બેન્ઝોઇક એસિડ
જ્યારે બેન્ઝીન હોમોલોગ્સ પોટેશિયમ પરમેંગેનેટ અને અન્ય મજબૂત ઓક્સિડેન્ટ્સના સંપર્કમાં આવે છે, ત્યારે બાજુની સાંકળો ઓક્સિડાઇઝ્ડ થાય છે. અવેજી સાંકળ કેટલી જટિલ છે, તે એ-કાર્બન અણુના અપવાદ સિવાય, નાશ પામે છે, જે કાર્બોક્સિલ જૂથમાં ઓક્સિડાઇઝ્ડ છે.
એક બાજુ સાંકળવાળા બેન્ઝીનના હોમોલોગ્સ બેંઝોઇક એસિડ આપે છે:
બે બાજુ સાંકળો ધરાવતાં હોમોલોગ્સ ડિબેસિક એસિડ આપે છે:
5 સી 6 એચ 5-સી 2 એચ 5 + 12 કેએમનો 4 + 18 એચ 2 એસઓ 4 → 5 સી 6 એચ 5 સીઓએચ + 5 સીઓ 2 + 6 કે 2 એસઓ 4 + 12 એમએનએસઓ 4 + 28 એચ 2 ઓ
5 સી 6 એચ 5-સીએચ 3 + 6 કેએમનો 4 + 9 એચ 2 એસઓ 4 → 5 સી 6 એચ 5 કોઓએચ + 3 કે 2 એસઓ 4 + 6 એમએનએસઓ 4 + 14 એચ 2 ઓ
સરળીકૃત :
સી 6 એચ 5-સીએચ 3 + 3 ઓ KMnO46 સી 6 એચ 5 સીઓઓએચ + એચ 2 ઓ
બી) બેંઝોઇક એસિડ ક્ષારથી તટસ્થ અને સહેજ આલ્કલાઇનમાં
સી 6 એચ 5-સીએચ 3 + 2KMnO 4 → સે 6 એચ 5 સીઓઓК + કે ОН + 2 એમએનઓ 2 + એચ 2 ઓ
II... વધારાની પ્રતિક્રિયાઓ (એલ્કનેસ કરતા સખત)
1. હેલોજેનેશન
સી 6 એચ 6 + 3 સીએલ 2 એચ ν 6 સી 6 એચ 6 સીએલ 6 (હેક્સાક્લોરોસાયક્લોહેક્ઝેન - હેક્સાક્લોરન)
2. હાઇડ્રોજન
સી 6 એચ 6 + 3 એચ 2 ટી , પં અથવા ની 6 સી 6 એચ 12 (સાયક્લોહેક્ઝેન)
3. પોલિમરાઇઝેશન
III. સબસ્ટિટ્યુશનલ રિએક્શન - આયનીય મિકેનિઝમ (એલ્કનેસ કરતા હળવા)
1. હેલોજેનેશન -
એ ) બેન્ઝિન
સી 6 એચ 6 + સીએલ 2 અલ.સી.એલ. 3 6 સી 6 એચ 5 -સીએલ + એચસીએલ (હરિતદ્રવ્ય)
સી 6 એચ 6 + 6 સીએલ 2 t, AlCl36 સે 6 સીએલ 6 + 6 એચસીએલ( હેક્સાક્લોરોબેનેઝિન)
સી 6 એચ 6 + બીઆર 2 t, FeCl36 સી 6 એચ 5 -બીઆર + એચબીઆર( બ્રોમોબેન્ઝિન)
બી) ઇરેડિયેશન અથવા હીટિંગ પર બેન્ઝિન હોમોલોગ્સ
રાસાયણિક ગુણધર્મની દ્રષ્ટિએ, એલ્કિલ રેડિકલ્સ એલ્કનેસ જેવા જ છે. તેમાંના હાઇડ્રોજન અણુને મુક્ત રેડિકલ મિકેનિઝમ દ્વારા હેલોજન દ્વારા બદલવામાં આવે છે. તેથી, હીટિંગ અથવા યુવી ઇરેડિયેશન પર ઉત્પ્રેરકની ગેરહાજરીમાં, આડ સાંકળમાં આમૂલ અવેજીની પ્રતિક્રિયા થાય છે. બેનઝિન રિંગની અસર એલ્કિલ અવેજીઓ પર થાય છે તે હકીકત તરફ દોરી જાય છે કાર્બન અણુ પરનો હાઇડ્રોજન અણુ સીધા જ બેન્ઝિન રિંગ (એક કાર્બન અણુ) સાથે બંધાયેલ છે હંમેશા બદલાઈ જાય છે.
1) સી 6 એચ 5-સીએચ 3 + સીએલ 2 એચ ν 6 સી 6 એચ 5-સીએચ 2 -સીએલ + એચસીએલ
સી) ઉત્પ્રેરકની હાજરીમાં બેન્ઝીનની હોમોલોગ્સ
સી 6 એચ 5-સીએચ 3 + સીએલ 2 અલ.સી.એલ. 3 . (Ort નું મિશ્રણ, ડેરિવેટિવ્ઝની જોડી) + HCl
2. નાઈટ્રેશન (નાઇટ્રિક એસિડ સાથે)
સી 6 એચ 6 + HO-NO 2 ટી, એચ 2 એસઓ 46 સી 6 એચ 5 -ન 2 2 એચ 2 ઓ
નાઇટ્રોબેન્ઝિન - ગંધ બદામ!
સી 6 એચ 5-સીએચ 3 + 3 એચઓ-નંબર 2 ટી, એચ 2 એસઓ 4→ થી એચ 3-સી 6 એચ 2 (કોઈ 2) 3 + 3 એચ 2 ઓ2,4,6-trinitrotoluene (tol, TNT)
બેન્ઝીન અને તેના હોમોલોગ્સનો ઉપયોગ
બેન્ઝિન સી 6 એચ 6 એ એક સારો દ્રાવક છે. બેંઝિન એડિટિવ તરીકે મોટર ઇંધણની ગુણવત્તામાં સુધારો કરે છે. ઘણા સુગંધિત કાર્બનિક સંયોજનોના ઉત્પાદન માટે કાચા માલ તરીકે સેવા આપે છે - નાઇટ્રોબેન્ઝિન સી 6 એચ 5 એનઓ 2 (દ્રાવક, એનિલિન તેમાંથી મેળવવામાં આવે છે), ક્લોરોબેન્ઝિન સી 6 એચ 5 સીએલ, ફિનોલ સી 6 એચ 5 ઓએચ, સ્ટાયરીન, વગેરે.
ટોલુએન સી 6 એચ 5 –CH 3 એ ડાયઝ, ડ્રગ્સ અને વિસ્ફોટકો (ટી.એન.ટી. (ટોલ), અથવા 2,4,6-ટ્રિનિટ્રોટોલ્યુએન ટી.એન.ટી.) ના ઉત્પાદનમાં વપરાય છે તે દ્રાવક છે.
ઝાયલેન્સસી 6 એચ 4 (સીએચ 3) 2. તકનીકી ઝાયલીન એ ત્રણ આઇસોમર્સનું મિશ્રણ છે ( ઓર્થો-, મેટા- અને દંપતી-ક્સ્લિનેસ) - ઘણા કાર્બનિક સંયોજનોના સંશ્લેષણ માટે દ્રાવક અને પ્રારંભિક ઉત્પાદન તરીકે ઉપયોગ થાય છે.
આઇસોપ્રોપીલબેન્ઝિન સી 6 એચ 5 –CH (સીએચ 3) 2 નો ઉપયોગ ફેનોલ અને એસીટોન મેળવવા માટે થાય છે.
બેન્ઝીનના ક્લોરિન ડેરિવેટિવ્ઝ છોડના રક્ષણ માટે વપરાય છે. તેથી, ક્લોરિન અણુઓ દ્વારા બેન્ઝિનમાં એચ અણુના અવેજીનું ઉત્પાદન હેક્સાક્લોરોબેન્ઝિન ene 6 Сl 6 છે - ફૂગનાશક; તેનો ઉપયોગ ઘઉંના સૂકા ડ્રેસિંગ માટે અને રાઈના દાણામાં સખત સ્મટ સામે થાય છે. બેંઝિનમાં ક્લોરિનના ઉમેરાનું ઉત્પાદન હેક્સાક્લોરોસાયક્લોહેક્ઝેન (હેક્સાચ્લોરન) સી 6 એચ 6 સીએલ 6 - જંતુનાશક છે; તેનો ઉપયોગ હાનિકારક જંતુઓને નિયંત્રણમાં કરવા માટે થાય છે. સૂક્ષ્મજીવો, છોડ અને પ્રાણીઓ સામે લડવા માટેના રાસાયણિક એજન્ટો - ઉલ્લેખિત પદાર્થો જંતુનાશકોના છે.
સ્ટાયરિન સી 6 એચ 5 - સીએચ \u003d સીએચ 2 પોલિમriરીઝ ખૂબ જ સરળતાથી, પોલિસ્ટરીન બનાવે છે, અને બૂટાડીઆન - સ્ટાયરીન બ્યુટાડીઅન રbersબર્સ સાથે કોપોલીમીરાઇઝિંગ.
વિડિઓ અનુભવો