กลุ่มแรกของปฏิกิริยา - ปฏิกิริยาการทดแทน เราบอกว่าสนามรบไม่มีพันธะหลายอย่างในโครงสร้างของโมเลกุล แต่มีระบบคอนจูเกตหกอิเล็กตรอนซึ่งมีเสถียรภาพมากและให้ความแข็งแรงเพิ่มเติมแก่แหวนเบนซิน ดังนั้นในปฏิกิริยาเคมีการเปลี่ยนอะตอมไฮโดรเจนนั้นเกิดขึ้นเป็นหลักและไม่ใช่การทำลายของแหวนเบนซิน
ด้วยปฏิกิริยาของการทดแทนเราพบเมื่อพูดคุยเกี่ยวกับอัลคอง แต่สำหรับพวกเขาปฏิกิริยาเหล่านี้ถูกเดินไปตามกลไกที่รุนแรงและกลไกของไอออนของปฏิกิริยาการทดแทนนั้นมีลักษณะโดยเวที
ครั้งแรกคุณสมบัติทางเคมี - ฮาโลเจน การเปลี่ยนอะตอมไฮโดรเจนบนอะตอมฮาโลเจน - คลอรีนหรือโบรมีน
ปฏิกิริยาถูกทำให้ร้อนและจำเป็นต้องมีการมีส่วนร่วมของตัวเร่งปฏิกิริยา ในกรณีของคลอรีนอาจเป็นอลูมิเนียมคลอไรด์หรือเหล็กคลอไรด์สาม ตัวเร่งปฏิกิริยาโพลาไรซ์โมเลกุลฮาโลเจนทำให้เกิดการหยุดการสื่อสารที่แตกต่างกันและมีไอออน
ชาร์จคลอรีนไอออนและตอบสนองด้วยเบนซีน
หากปฏิกิริยาเกิดขึ้นกับโบรมีนดังนั้นตัวเร่งปฏิกิริยาคือโบรไมด์เหล็กสามหรืออลูมิเนียมโบรไมด์

เป็นสิ่งสำคัญที่จะต้องทราบว่าปฏิกิริยาเกิดขึ้นกับโบรมอกโมเลกุลและไม่ใช่กับน้ำโบรมีน ด้วยน้ำโบรมีนเบนซีนไม่ตอบสนอง
Halogenation of Gomologists Benzene มีลักษณะของตัวเอง ในโมเลกุลโทลูอีนกลุ่มเมธิลอำนวยความสะดวกในการทดแทนในวงแหวนการเกิดปฏิกิริยาเพิ่มขึ้นและปฏิกิริยาที่เกิดขึ้นภายใต้สภาวะที่ไม่รุนแรงนั่นคือที่อุณหภูมิห้อง

เป็นสิ่งสำคัญที่จะต้องทราบว่าการทดแทนเกิดขึ้นเสมอในตำแหน่ง ortho- และคู่ดังนั้นจึงมีการผสมผสานของไอโซเมอร์
ประการที่สองอสังหาริมทรัพย์ - ไนเตรทเบนซินการแนะนำของกลุ่มไนโตรเป็นแหวนเบนซิน
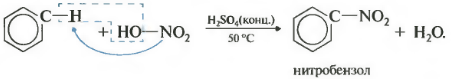
ของเหลวสีเหลืองหนักที่มีกลิ่นของอัลมอนด์ขมเกิดขึ้น - Nitrobenzene ดังนั้นปฏิกิริยาสามารถมีคุณภาพสูงบนเบนซิน สำหรับเกลียวส่วนผสมไนเตรตของกรดไนตริกและกรดซัลฟูริกเข้มข้น ปฏิกิริยาจะถูกดำเนินการเมื่อได้รับความร้อน
ให้ฉันเตือนคุณว่าสำหรับ nitration ของ Alkanans ในปฏิกิริยาของ Konovalov, เจือจางกรดไนตริกถูกใช้โดยไม่ต้องเพิ่มกำมะถัน
ในเกลียวของโทลูอีนรวมถึงในช่วงฮาโลเจนส่วนผสมของ ortho- และพารามิเตอร์จะเกิดขึ้น

ประการที่สามคุณสมบัติ - Alkylation ของเบนซีนเฮลาลิน

ปฏิกิริยานี้ช่วยให้คุณสามารถแนะนำหัวรุนแรงไฮโดรคาร์บอนเป็นแหวนเบนซินและถือได้ว่าเป็นวิธีการผลิต Benzene Homologs อลูมิเนียมคลอไรด์ใช้เป็นตัวเร่งปฏิกิริยาที่ส่งเสริมการสลายตัวของโมเลกุลฮาโลเจนกับไอออน ยังต้องใช้ความร้อน
ที่สี่คุณสมบัติ - Alkylation ของ Benzene Alkenes
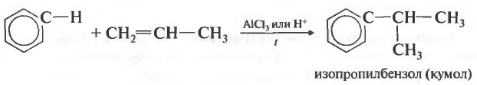
ด้วยวิธีนี้มันเป็นไปได้ที่จะได้รับตัวอย่างเช่นคิวลหรือเอทิลเบนซีน ตัวเร่งปฏิกิริยา - อลูมิเนียมคลอไรด์
2. ปฏิกิริยาที่แนบมากับเบนซีน
กลุ่มที่สองของปฏิกิริยา - ปฏิกิริยาของสิ่งที่แนบมา เรากล่าวว่าปฏิกิริยาเหล่านี้ไม่ได้เป็นลักษณะ แต่เป็นไปได้ที่สภาพคงที่ที่เพียงพอกับการทำลายเมฆ PI-Electronic และการก่อตัวของ Six Sigma Bonds
ที่ห้าคุณสมบัติในรายการโดยรวมคือการเติมไฮโดรเจนการเติมไฮโดรเจน
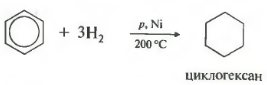
อุณหภูมิความดันนิกเกิลหรือตัวเร่งปฏิกิริยาแพลทินัม ในลักษณะเดียวกันโทลูอีนสามารถทำปฏิกิริยาตอบสนองได้
ที่หกคุณสมบัติ - คลอรีน โปรดทราบว่าเรากำลังพูดถึงการมีปฏิสัมพันธ์กับคลอรีนเนื่องจากโบรมีนไม่ได้เข้าสู่ปฏิกิริยานี้
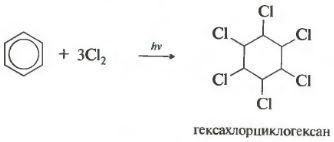
ปฏิกิริยาตอบสนองด้วยการฉายรังสีอัลตราไวโอเลตที่เข้มงวด Hexachlorcyclohexane ก่อตั้งขึ้นชื่อ Hexachlororan อื่นซึ่งเป็นของแข็ง
เป็นสิ่งสำคัญที่ต้องจำไว้ว่าสำหรับเบนซีน เป็นไปไม่ได้ ปฏิกิริยาของการเพิ่มไฮโดรเจนฮาโลเจน Sodes (Hydro-aliation) และการเชื่อมต่อน้ำ (ชุ่มชื้น)
3. การเปลี่ยนในห่วงโซ่ด้านข้างของ Benzene Homologues
กลุ่มที่สามของปฏิกิริยาที่เกี่ยวข้องกับ Benzene Homologuse เท่านั้น - นี่คือการทดแทนในห่วงโซ่ด้านข้าง
ที่เจ็ดทรัพย์สินในรายการโดยรวมคือฮาโลเจนตามอัลฟาคาร์บอนในห่วงโซ่ด้านข้าง
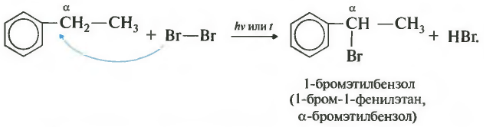
ปฏิกิริยาเกิดขึ้นเมื่อได้รับความร้อนหรือฉายรังสีและมักจะมีเพียงอัลฟาคาร์บอน ด้วยความต่อเนื่องของฮาโลเจนอะตอมฮาโลเจนที่สองจะเพิ่มขึ้นอีกครั้งในตำแหน่งอัลฟ่า
4. ออกซิเดชันของ benzene homologues
กลุ่มที่สี่ของปฏิกิริยา - ออกซิเดชัน
แหวนเบนซินนั้นทนทานเกินไปดังนั้นเบนซีนจึง อย่าออกซิไดซ์ Permanganate โพแทสเซียม - ไม่เปลี่ยนสีโซลูชันของมัน มันสำคัญมากที่ต้องจำไว้
แต่ Gomologists ของเบนซีนเกิดออกซิไดซ์โดยสารละลายโพแทสเซียมที่ทำให้เป็นกรดเมื่อถูกความร้อน และนี่คือคุณสมบัติทางเคมีที่แปด
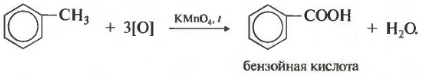
ปรากฎว่ากรดเบนโซอิก มีการเปลี่ยนสีของการแก้ปัญหา ในเวลาเดียวกันไม่ว่าห่วงโซ่คาร์บอนจะใช้เวลานานเท่าใดก็จะเกิดขึ้นหลังจากอะตอมคาร์บอนแรกและอัลฟาอะตอมถูกออกซิไดซ์ไปยังกลุ่มคาร์บอกซิลที่มีการก่อตัวของกรดเบนโซอิก ส่วนที่เหลือของโมเลกุลจะออกซิไดซ์ไปยังกรดที่เหมาะสมหรือถ้ามันเป็นเพียงหนึ่งอะตอมคาร์บอนไดออกไซด์คาร์บอนไดออกไซด์
หากนักโกฏิมของเบนซีนมีไฮโดรคาร์บอนมากกว่าหนึ่งตัวในวงแหวนที่มีกลิ่นหอมเกิดจากการเกิดออกซิเดชันตามกฎเดียวกัน - คาร์บอนจะออกซิไดซ์ในตำแหน่งอัลฟ่า

ในตัวอย่างนี้ได้รับกรดอะโรมาติกสองแบบซึ่งเรียกว่ากรด phthalic
ในวิธีพิเศษฉันจะสังเกตเห็นออกซิเดชั่นของ Cumol, Isopropylbenzene, ออกซิเจนในอากาศในการปรากฏตัวของกรดซัลฟิวริก

นี่คือวิธีการเชื่อมต่อที่เรียกว่าการได้รับฟีนอล ตามกฎแล้วจำเป็นต้องเผชิญกับปฏิกิริยานี้ในเรื่องที่เกี่ยวข้องกับการรับฟีนอล นี่เป็นวิธีอุตสาหกรรม
เก้าอสังหาริมทรัพย์ - การเผาไหม้ออกซิเจนออกซิเดชั่นที่สมบูรณ์ Benzole และ homologs เผาไหม้คาร์บอนไดออกไซด์และน้ำ
เราเขียนสมการของการเผาไหม้ของเบนซีนโดยทั่วไป
ภายใต้กฎหมายของการรักษามวลของอะตอมด้านซ้ายควรจะมากเท่ากับอะตอมที่อยู่ทางขวา เพราะหลังจากทั้งหมดในปฏิกิริยาเคมีอะตอมไม่ได้ไปที่ใดก็ได้ แต่เพียงแค่เปลี่ยนลำดับของการเชื่อมต่อระหว่างพวกเขา ดังนั้นโมเลกุลคาร์บอนไดออกไซด์จะมากเท่ากับอะตอมคาร์บอนในโมเลกุลของยานพาหนะเนื่องจากอะตอมคาร์บอนหนึ่งกระบอกสูบรวมถึงองค์ประกอบของโมเลกุล นั่นคือ N Molecules CO 2 โมเลกุลของน้ำจะน้อยกว่าอะตอมไฮโดรเจนนั่นคือ (2N-6) / 2 ซึ่งหมายถึง N-3
อะตอมออกซิเจนที่ด้านซ้ายและขวาของจำนวนเดียวกัน ทางด้านขวาของพวกเขา 2N จากคาร์บอนไดออกไซด์เพราะในแต่ละโมเลกุลอะตอมออกซิเจนสองตัวรวมถึง N-3 ของน้ำและ 3N-3 ด้านซ้ายของอะตอมออกซิเจนเหมือนกัน - 3n-3 ซึ่งหมายถึงโมเลกุลน้อยกว่าสองเท่าเนื่องจากองค์ประกอบของโมเลกุลมีอะตอมสองครั้ง นั่นคือ (3n-3) / 2 โมเลกุลออกซิเจน
ดังนั้นเราจึงประกอบด้วยสมการการเผาไหม้ของ Benzene Homologues โดยทั่วไป
SPVSH (F) FGBOU VPO
แผนก "ความปลอดภัยจากอัคคีภัย"
ทดสอบ
ภายใต้วินัย "ทฤษฎีการเผาไหม้และการระเบิด"
หมายเลขงาน 1
กำหนดปริมาณทางทฤษฎีเฉพาะและปริมาณอากาศที่จำเป็นสำหรับการเผาไหม้เต็มรูปแบบของไอเบนซีน เงื่อนไขที่มีอากาศอยู่ที่อุณหภูมิของทีวีและความดันของ PB และคู่ของเบนซีน - อุณหภูมิของ TG และความดันของ rg ผลการคำนวณเพื่อแสดงในหน่วยต่อไปนี้:; ;;;
ข้อมูลต้นฉบับ (N - หมายเลขกลุ่ม N - หมายเลขในรายการของนักเรียน:
TV \u003d 300 + (- 1) n * 2 * n - (- 1) n * 0.2 * n \u003d 277.6 k
pv \u003d? 10 3 \u003d 95900 pa;
tg \u003d 300? (? 1) n? 2? n? (? 1) n? 0,2? n \u003d 321.6 k;
PR \u003d? 10 3 \u003d 79400 pa
C6H6 + 7,5O2 + 7,5? 3,76N2 \u003d 6CO2 + 3PO + 7,5? 3.76N2 + QP (1),
ที่ Q - ความร้อนของปฏิกิริยาเคมี จากสมการนี้เป็นไปได้ที่จะกำหนดค่าสัมประสิทธิ์ stoichiometric ของน้ำมันเบนซินและออกซิเจนโมเลกุล: vg \u003d 1, v0 \u003d 7.5
2. ปริมาณทางทฤษฎีที่เฉพาะเจาะจงของอากาศคือจำนวนกิโลเมตรอากาศที่จำเป็นสำหรับการเผาไหม้ที่สมบูรณ์ของเบนซินหนึ่งกิโลเมตรคำนวณโดยสูตร:
ที่ 4.76 คือปริมาณอากาศที่มีหน่วยของปริมาณออกซิเจน \u003d - อัตราส่วนของค่าสัมประสิทธิ์ stoichiometric ของออกซิเจนโมเลกุล (VO) และเบนซิน (VG)
การแทนที่ใน (d) ค่า VO และ VG เราได้รับ:
3. ปริมาณอากาศที่จำเป็นสำหรับการเผาไหม้ที่สมบูรณ์ของน้ำมันเบนซินหนึ่งกิโลเมตรถูกกำหนดดังนี้:
ปริมาณของอากาศหนึ่งกิโลเมตรที่อุณหภูมิทีวีและความดันของ RV ค่าคำนวณโดยสูตร
ที่ 22.4 เป็นปริมาณของก๊าซกรามภายใต้สภาวะปกติ PO \u003d 101325 PA - ความดันปกติจากนั้น \u003d 273 K เป็นอุณหภูมิปกติ
การทดแทนทีวีจากนั้น RV, RO ใน (5) เราได้รับ
ปริมาณทางทฤษฎีเฉพาะของอากาศคำนวณโดยสูตร (4):
4. ปริมาณอากาศการเผาไหม้ที่สมบูรณ์แบบที่จำเป็นของหน่วยของปริมาณของเชื้อเพลิงก๊าซถูกกำหนดดังนี้:
ปริมาณของเชื้อเพลิงหนึ่งกิโลเมตร - ไอเบนซีนที่อุณหภูมิของ TG และแรงดันของ rg พิจารณาว่า
และการทดแทน (8) และ (5) ใน (7) เราได้รับนิพจน์ต่อไปนี้สำหรับปริมาณอากาศตามทฤษฎีที่เฉพาะเจาะจง:
คำนวณค่าของพารามิเตอร์กระบวนการเผาไหม้นี้:
ปริมาณอากาศที่จำเป็นสำหรับการเผาไหม้ที่สมบูรณ์ของน้ำมันเบนซินหนึ่งกิโลกรัมถูกกำหนดเป็น:
ที่ไหน - มวลกรามของเชื้อเพลิง - มวลของเบนซีนหนึ่งกิโลเมตรแสดงเป็นกิโลกรัม น้ำหนักไฝของน้ำมันเบนซินเท่ากับน้ำหนักโมเลกุลในสูตร:
AC? NC + An? Nn, UIAI? Ni (11)
ที่ AC และน้ำหนักอะตอมของคาร์บอนและไฮโดรเจน, NC และ NN - จำนวนอะตอมคาร์บอนในโมเลกุลเบนซีน การแทนที่ค่าของ AC \u003d 12, NC \u003d 6, AN \u003d 1, NN \u003d 6 เราได้รับ:
ปริมาณทางทฤษฎีทางทฤษฎีที่เฉพาะเจาะจงเราพบว่าแทนที่ค่าของ n ในและในสูตร (10):
ผลของการคำนวณ:
หมายเลขงานที่ 2
กำหนดจำนวนเงินตามทฤษฎีที่เฉพาะเจาะจงปริมาณและองค์ประกอบของผลิตภัณฑ์การเผาไหม้ของเบนซีนหากค่าสัมประสิทธิ์ของอากาศส่วนเกินอุณหภูมิของ TP และความดันของผลิตภัณฑ์เผาไหม้ RP อุณหภูมิของ TG และความดันของถั่ว ของเบนซีน ผลของการคำนวณเพื่อแสดงในเศษส่วนกราม (เป็นเปอร์เซ็นต์) และในหน่วยต่อไปนี้:; ;;
ข้อมูลเริ่มต้น:
b \u003d 1.5 + (? 1) n? 0.1? n? (? 1) n? 0.01? n \u003d 0.2;
rp \u003d 10 3 \u003d 68400 pa;
TP \u003d 1600 (? 1) n? 20? n? (? 1) n? 2? n \u003d 1816 k;
TG \u003d 273? (? 1) n? 2? n + (? 1) n? 0,2? n \u003d 295.4 k;
rg \u003d 10 3 \u003d 111600 pa;
โซลูชัน (n \u003d 11, n \u003d 2)
1. เราเขียนสมการ stoichiometric ของปฏิกิริยาของการเผาไหม้ของเบนซีนในอากาศ:
C 6 H 6 + 7,5O 2 +7,5? 3,76N 2 \u003d 6CO 2 + 3H 2 O + 7,5? 3.76N 2 + QP, (1)
ที่ QP คือความร้อนของปฏิกิริยาเคมี จากสมการนี้เรากำหนดค่าสัมประสิทธิ์ stoichiometric ต่อไปนี้:
V CO2 \u003d 6, V PO \u003d 3, V C6H6 \u003d 1, V O2 \u003d 7.5, V N2 \u003d 7,5? 3.76
2. กำหนดปริมาณการเผาไหม้ของผลิตภัณฑ์เผาไหม้หนึ่งกิโลเมตรของเชื้อเพลิง:
การทดแทนใน (2) ค่าของค่าสัมประสิทธิ์ stoichiometric ของผลิตภัณฑ์การเผาไหม้และเชื้อเพลิงเราได้รับ:
3. ปริมาณทางทฤษฎีเฉพาะของอากาศคือจำนวนกิโลเมตรที่จำเป็นสำหรับการเผาไหม้ที่สมบูรณ์ของเชื้อเพลิงหนึ่งกิโลเมตรเรากำหนดด้วยความช่วยเหลือของสูตร:
ที่ 4.76 คือปริมาณอากาศที่หน่วยออกซิเจนมีอยู่
อัตราส่วนของค่าสัมประสิทธิ์ Stoichiometric ของออกซิเจนโมเลกุลและเบนซีน
การแทนที่ใน (4) ค่า v o2 \u003d 7.5 และ v c6h6 \u003d 1, เราได้รับ:
4. อากาศส่วนเกินที่บัญชีสำหรับเชื้อเพลิง 1 กิโลเมตรถูกกำหนดโดยการแสดงออก:
เบนซีนคู่เผาไหม้อากาศ
การแทนที่ในการแสดงออกนี้
37,7(0,2-1)=30,16(7)
5. จำนวนรวมของหน่วยผลิตภัณฑ์เผาไหม้ของปริมาณน้ำมันเชื้อเพลิงถูกกำหนดโดยจำนวนเงิน:
หลังจากทดแทนค่าและรับ:
6. หุ้นกรามของผลิตภัณฑ์เผาไหม้ที่แสดงเป็นเปอร์เซ็นต์จะถูกกำหนดดังนี้:
ในสูตร (9) สำหรับเศษส่วนกรามของไนโตรเจนและออกซิเจนในผลิตภัณฑ์เผาไหม้ 0.79 และ 0.21 - เศษฟันกรามของสารเหล่านี้ในอากาศส่วนเกินซึ่งนำไปสู่การเพิ่มขึ้นของส่วนแบ่งของไนโตรเจนและลักษณะของออกซิเจนในการเผาไหม้ผลิตภัณฑ์ .
7. เพื่อกำหนดปริมาณเฉพาะและผลิตภัณฑ์การเผาไหม้ที่เฉพาะเจาะจงมีความจำเป็นต้องคำนวณปริมาณฟันกรามของพวกเขา - ปริมาตรของก๊าซหนึ่งกิโลเมตรภายใต้เงื่อนไขที่ผลิตภัณฑ์ตั้งอยู่:
ที่ 22.4 คือปริมาณของก๊าซหนึ่งกิโลเมตรภายใต้สภาวะปกติ T 0 \u003d 273k - อุณหภูมิปกติ RO \u003d 1013255 - ความดันปกติ
การทดแทนใน (10) ค่า RO แล้วเราได้รับ:
ปริมาณของผลิตภัณฑ์ที่เกิดขึ้นในระหว่างการเผาไหม้ของเชื้อเพลิงหนึ่งกิโลกรัมไม่รวมอากาศส่วนเกินคำนวณดังนี้:
ที่ไหน - มวลกรามของเชื้อเพลิง - มวลของเบนซีนหนึ่งกิโลเมตรแสดงเป็นกิโลกรัม มวลโมลของเบนซีนอยู่ในสูตร:
ที่ AC และ AS เป็นน้ำหนักอะตอมของคาร์บอน (12) และไฮโดรเจน (1), N C และ N - จำนวนอะตอมคาร์บอน (6) และไฮโดรเจน (6) ในเหมืองเบนซีน (จาก 6 ชั่วโมง 6)
การแทนที่ค่าและใน (12) เราได้รับ
ปริมาณอากาศส่วนเกินต่อ 1 กิโลกรัมของเชื้อเพลิงถูกกำหนด:
ปริมาณของอากาศส่วนเกินหนึ่งกิโลเมตรซึ่งตั้งอยู่ในผลิตภัณฑ์เผาไหม้ เนื่องจากอุณหภูมิและความดันของอากาศส่วนเกินสอดคล้องกับอุณหภูมิและความดันของผลิตภัณฑ์ของการเผาไหม้แล้ว \u003d \u003d 220.7
การแทนที่ค่านี้และใน (14) เราได้รับ:
ในการคำนวณปริมาณผลิตภัณฑ์การเผาไหม้เชื้อเพลิงที่เฉพาะเจาะจงเราจะสมมติว่าคู่เบนซินมีอุณหภูมิของ TG ที่ความดัน:
ปริมาณของหนึ่งกิโลเมตรของไอน้ำมันเบนซินที่อุณหภูมิของ TG และความดันของ WG ปริมาณน้ำมันฟันกรามคำนวณโดยสูตร:
การทดแทนค่าที่ได้รับและค่าดังกล่าวและใน (17) เราได้รับ:
ปริมาณอากาศส่วนเกินต่อลูกบาศก์เมตรของไอเบนซีนไอถูกกำหนดดังนี้:
การเปลี่ยนตัวใน (20) ค่า \u003d 30,16, \u003d และ
ให้ผลลัพธ์ต่อไปนี้:
ปริมาณเฉพาะของผลิตภัณฑ์การเผาไหม้โดยคำนึงถึงส่วนเกินของอากาศจะถูกกำหนดโดยผลรวม
ผลของการคำนวณ:
x co2 \u003d%; x H2O \u003d 4.4%; x n2 \u003d%; x o2 \u003d 11.7%
เอกสารที่คล้ายกัน
การคำนวณค่าสัมประสิทธิ์การติดไฟของ Nitrobenzene C6H5NO2 และ CS2 Serougerod สมการของปฏิกิริยาของการเผาไหม้ propylate acetate ในอากาศ การคำนวณผลิตภัณฑ์อากาศและการเผาไหม้ในระหว่างการเผาไหม้ของก๊าซที่ติดไฟได้ การกำหนดอุณหภูมิแฟลชโทลูอีนตามสูตร V. Blinov
การตรวจสอบเพิ่ม 04/08/2017
การคำนวณปริมาณอากาศและผลิตภัณฑ์การเผาไหม้ที่เกิดขึ้นในระหว่างการเผาไหม้ของสาร สมการของปฏิกิริยาการเผาไหม้ของเอทิลีนไกลคอลในอากาศ การเผาผลาญของก๊าซที่ติดไฟได้ การคำนวณอุณหภูมิการเผาไหม้ adiabatic สำหรับส่วนผสม stoichiometric การเผาไหม้ของ Propanol
การตรวจสอบเพิ่ม 10/17/2012
มุมมองของการเผาไหม้และพารามิเตอร์หลัก การเปลี่ยนแปลงทางเคมีของน้ำมันเชื้อเพลิงและสารออกซิไดซ์ในผลิตภัณฑ์การเผาไหม้ สมการของวัสดุและความสมดุลของความร้อนของปฏิกิริยาการเผาไหม้ ผลกระทบของสัมประสิทธิ์อากาศส่วนเกินในองค์ประกอบของผลิตภัณฑ์การเผาไหม้และอุณหภูมิการเผาไหม้
การตรวจสอบเพิ่ม 01/17/2013
ความมุ่งมั่นของปริมาณอากาศที่จำเป็นสำหรับการเผาไหม้ที่สมบูรณ์ของหน่วยของสารที่ติดไฟได้ องค์ประกอบของผลิตภัณฑ์การเผาไหม้ของมวลของสารที่ติดไฟได้ ข้อ จำกัด ของการแพร่กระจายของเปลวไฟของก๊าซ, ไอน้ำ, ส่วนผสมที่เต็มไปด้วยฝุ่น แรงดันขยายระเบิด
หลักสูตร, เพิ่ม 12/23/2013
การพัฒนามาตรการเพื่อป้องกันการเกิดไฟไหม้และการระเบิดการประเมินเงื่อนไขการพัฒนาและปราบปราม แนวคิดของความเร็วของความเหนื่อยหน่ายวิธีการของคำจำกัดความของมัน ขั้นตอนการรวบรวมสมการปฏิกิริยาการเผาไหม้ การคำนวณปริมาณอากาศที่จำเป็นสำหรับไฟไหม้
หลักสูตร, เพิ่ม 07/10/2014
การกำหนดองค์ประกอบของผลิตภัณฑ์ของการเผาไหม้เต็มรูปแบบของก๊าซ การคำนวณอุณหภูมิการเผาไหม้แบบอะเดียแบติกของส่วนผสมของก๊าซในปริมาณคงที่และความดันคงที่ ค่าคงที่ปฏิกิริยา Kinetic ของก๊าซธรรมชาติที่ติดไฟเอง ขีด จำกัด ของการจุดระเบิดของส่วนผสมของก๊าซ
งานหลักสูตรเพิ่มใน 19.02.2014
ลักษณะของวิธีการอุตสาหกรรมของ Alkylation ของโพรพิลีนเบนซิน หลักการของ Alkylation ของเบนซีนโอเลฟินส์ในเทคโนโลยีเคมี ปัญหาการออกแบบพืชเทคโนโลยีของอัลคลอเนชั่นเบนซีน คำอธิบายของกระบวนการผลิตเทคโนโลยี
วิทยานิพนธ์เพิ่ม 11/15/2010
การเผาไหม้เป็นกระบวนการออกซิเดชั่นที่ทรงพลัง ประเภทของการเผาไหม้: เสียงเรียกเข้าและการเผาไหม้ด้วยเปลวไฟ การระเบิดเป็นกรณีพิเศษของการเผาไหม้ คุณสมบัติเปลวไฟไฟฟ้า ความหลากหลายของผลิตภัณฑ์การเผาไหม้อันเป็นผลมาจากการเผาไหม้เชื้อเพลิงที่ไม่สมบูรณ์ การกรองควันผ่านน้ำ
งานทางวิทยาศาสตร์เพิ่ม 07/29/2009
การกำหนดปริมาณของอากาศที่จำเป็นสำหรับการเผาไหม้ที่สมบูรณ์ของปริมาณโพรเพนที่ระบุ การคำนวณการเปลี่ยนแปลงใน Enthalpy, เอนโทรปีและพลังงานของกิ๊บส์ด้วยความช่วยเหลือของผลที่ตามมาของกฎหมาย GESS การกำหนดมวลฟันกรามของการเทียบเท่าของสารออกซิไดซ์และตัวแทนลด
การตรวจสอบเพิ่ม 08.02.2012
วิธีการในการกำหนดปริมาณการใช้น้ำมันดูดซับความเข้มข้นของเบนซีนในการดูดซับน้ำมันออกจากโช้ค การคำนวณเส้นผ่าศูนย์กลางและความสูงของหัวฉีดโช้ค ความมุ่งมั่นของพื้นผิวความร้อนที่ต้องการในคอลัมน์คิวบาและการใช้ไอน้ำความร้อน
AROMATOM WC (อารีน่า) - นี่คือ HC ที่โมเลกุลมีวงแหวนเบนซินหนึ่งอันขึ้นไป
ตัวอย่างของ HC หอม:

Arena ของเบนซีนจำนวนหนึ่ง (Monocyclic Arena)
สูตรทั่วไป:c n h 2n-6, n≥6
ตัวแทนที่ง่ายที่สุดของ AROMATOM HC คือเบนซินสูตรเชิงประจักษ์ที่มี 6 ชั่วโมง 6
โครงสร้างอิเล็กทรอนิกส์ของโมเลกุลเบนซีน
สูตรทั้งหมดของ Monocyclic Arena C N H 2 N -6 แสดงให้เห็นว่าพวกเขาเป็นสารประกอบที่ไม่อิ่มตัว
ในปี 1856 นักเคมีชาวเยอรมัน A.F. Kekule แนะนำสูตรที่เป็นวงจรของเบนซีนด้วยการเชื่อมต่อคอนจูเกต (พันธะที่เรียบง่ายและคู่อื่น ๆ ) - Cyclohexitrien-1,3,5: 
โครงสร้างดังกล่าวของโมเลกุลเบนซีนไม่ได้อธิบายคุณสมบัติมากมายของเบนซีน:
- สำหรับเบนซีนปฏิกิริยาการทดแทนเป็นลักษณะและไม่ใช่ปฏิกิริยาของลักษณะที่แนบมาของสารประกอบที่ไม่อิ่มตัว ปฏิกิริยาของสิ่งที่แนบมาเป็นไปได้ แต่มันก็ยากกว่า;
- benzole ไม่ตอบสนองซึ่งเป็นปฏิกิริยาที่มีคุณภาพสูงต่อ HC ที่ไม่อิ่มตัว (พร้อมกับน้ำโบรมีนและสารละลายของ KMNO 4)
การศึกษาทางอิเล็กทรอนิกส์ที่จัดขึ้นในภายหลังแสดงให้เห็นว่าการเชื่อมโยงทั้งหมดระหว่างอะตอมคาร์บอนในโมเลกุลเบนซีนมีความยาวเท่ากัน 0.140 นาโนเมตร (ค่าเฉลี่ยระหว่างความยาวเป็นเรื่องง่าย การเชื่อมต่อ C-S 0.154 nm และพันธะคู่กับ \u003d กับ 0.134 nm) มุมระหว่างการเชื่อมต่อในแต่ละอะตอมคาร์บอนคือ 120 o โมเลกุลเป็นหกเหลี่ยมที่ถูกต้อง
ทฤษฎีสมัยใหม่สำหรับการอธิบายโครงสร้างของโมเลกุล C 6 H 6 ใช้แนวคิดของการผสมผสานของ Orom Orbitals
อะตอมคาร์บอนในเบนซีนอยู่ในสถานะของ SP 2-Hybridization อะตอม "C" แต่ละอันในรูปแบบสามข้อผูกพัน (สองด้วยอะตอมคาร์บอนและหนึ่งที่มีอะตอมไฮโดรเจน) พันธบัตรσทั้งหมดอยู่ในระนาบเดียวกัน:
อะตอมคาร์บอนแต่ละกระบอกมีหนึ่ง P-Electron ซึ่งไม่เกี่ยวข้องกับการผสมผสาน annbridized p-orbitals ของอะตอมคาร์บอนอยู่ในระนาบตั้งฉากกับระนาบของลิงค์σ แต่ละ p-cloud ทับซ้อนกับสอง p-clouds ที่อยู่ติดกันและเป็นผลให้ระบบคอนจูเกตเดียวเกิดขึ้น (จำผลกระทบของการผันพ่น P-electrons ในโมเลกุล bitadiethine-1,3 พิจารณาในรูปแบบ "dien ไฮโดรคาร์บอน "):
การรวมกันของหกσ-bonds ที่มีระบบหนึ่งπเรียกว่า พันธะหอม
วัฏจักรของอะตอมคาร์บอนหกชิ้นที่เกี่ยวข้องกับพันธะหอมเรียกว่า แหวนเบนซินหรือ นิวเคลียสเบนซิน.
สอดคล้องกับแนวคิดที่ทันสมัยเกี่ยวกับโครงสร้างอิเล็กทรอนิกส์ของเบนซีนโมเลกุลของ 6 H 6 นั้นแสดงให้เห็นดังต่อไปนี้:

คุณสมบัติทางกายภาพของเบนซีน
เบนซีนภายใต้สภาวะปกติ - ของเหลวไม่มีสี t o pl \u003d 5.5 ° C; t o kip \u003d 80 o c; มีกลิ่นลักษณะ; มันไม่ได้ผสมกับน้ำตัวทำละลายที่ดีเป็นพิษอย่างรุนแรง
คุณสมบัติทางเคมีของเบนซีน
การสื่อสารที่มีกลิ่นหอมกำหนดคุณสมบัติทางเคมีของเบนซีนและ HC ที่มีกลิ่นหอมอื่น ๆ
ระบบอิเล็กทรอนิกส์6πมีความเสถียรมากกว่าพันธบัตรสองแบบสามัญไฟฟ้า ดังนั้นปฏิกิริยาของสิ่งที่แนบมาจึงมีลักษณะน้อยกว่า HC ที่มีกลิ่นหอมมากกว่า HC ที่ไม่อิ่มตัว ลักษณะส่วนใหญ่ของเวทีคือปฏิกิริยาของการทดแทน
ผม.. ปฏิกิริยาการทดแทน
1. ครึ่งหนึ่ง

2. ไนเตรท
ปฏิกิริยาจะดำเนินการโดยส่วนผสมและกรด (ส่วนผสมของไนตริน): 
3.sulfing

4. แอคไลท์ (แทนที่อะตอม "H" ในกลุ่มอัลคิล) - ปฏิกิริยา Freidel-Kraftsgomezol homologues เกิดขึ้น:

แทนที่จะใช้ Alleasan ฮาโลเจน, Alkenes สามารถใช้ (ต่อหน้าตัวเร่งปฏิกิริยา - ALCL 3 หรือกรดอนินทรีย์):

ครั้งที่สอง. ปฏิกิริยาของการเข้าร่วม
1. อุทกศาสตร์

2. คลอรีนมาถึง

สาม. ปฏิกิริยาออกซิเดชั่น
1. การเผาไหม้
2C 6 H 6 + 15O 2 → 12SO 2 + 6N 2
2. ออกซิเดชันที่ไม่สมบูรณ์ (KMNO 4 หรือ K 2 CR 2 O 7 ในสภาพแวดล้อมที่เป็นกรด) แหวนเบนซินมีความทนทานต่อสารออกซิไดซ์ ปฏิกิริยาไม่เกิดขึ้น
รับเบนซีน
ในอุตสาหกรรม:
1) การกลั่นน้ำมันและถ่านหิน
2) cyclohexane dehydrogenation:

3) dehydrocyclization (aromatization) ของ hexane:

ในห้องปฏิบัติการ:
กลิ้งเกลือกรดเบนโซอิกจาก:

Isomeria และการตั้งชื่อของ Benzene Homologues
นักโกฏนวิทยาของเบนซีนใด ๆ มีห่วงโซ่ด้านข้าง I.e. alkyl อนุมูลอิสระที่เกี่ยวข้องกับแกนเบนซิน นักเดินเล่นคนแรกของเบนซีนเป็นแกนเบนซินที่เกี่ยวข้องกับเมธิลอนุมูล: 
โทลูอีนไม่มีไอโซเมอร์เนื่องจากบทบัญญัติทั้งหมดในแกนเบนซินนั้นเท่ากัน
สำหรับ homologs ที่ตามมาของเบนซีนชนิดหนึ่งของ isomerism เป็นไปได้ - isomeria ของโซ่ด้านข้างซึ่งสามารถเป็นสองประเภท:
1) isomeria ของจำนวนและโครงสร้างของ substituents;
2) isomerization ของตำแหน่งของแหล่งย่อย



คุณสมบัติทางกายภาพ toloole
โทลูอีน - ของเหลวไม่มีสีที่มีกลิ่นลักษณะไม่ละลายในน้ำที่ละลายได้ดีในตัวทำละลายอินทรีย์ โทลูอีนมีพิษน้อยกว่าเบนซีน
คุณสมบัติทางเคมีของ Toloola
ผม.. ปฏิกิริยาการทดแทน
1. ปฏิกิริยากับการมีส่วนร่วมของแหวนเบนซิน
Methylbenzene เข้าสู่ปฏิกิริยาการทดแทนทั้งหมดที่มีส่วนเกี่ยวข้องกับเบนซีนและแสดงความจุของปฏิกิริยาที่สูงขึ้นปฏิกิริยาการไหลด้วยความเร็วที่มากขึ้น
Methyl Radical ที่มีอยู่ในโมเลกุล Toluene เป็นสารแทนที่จะเป็นผลมาจากปฏิกิริยาของการทดแทนในแกนเบนซิน, Ortho- และ Para-Derivatives ของโทลูอีนจะได้รับหรือส่วนเกินของรีเอเจนต์ - Tripper ผลิตทั่วไป สูตร:

a) ฮาโลเจน


ด้วยคลอรีนเพิ่มเติม Dichloromethylbenzene และ Trichloromethylbenzene:

ครั้งที่สอง. ปฏิกิริยาของการเข้าร่วม
การไฮโดรเจน

สาม.ปฏิกิริยาออกซิเดชั่น
1.
C 6 H 5 CH 3 + 9O 2 → 7CO 2 + 4H 2 O
2. ออกซิเดชันที่ไม่สมบูรณ์
ตรงกันข้ามกับเบนซีน homologs ของเขาออกซิไดซ์โดยสารออกซิไดซ์บางส่วน; ในเวลาเดียวกันห่วงโซ่ด้านข้างจะถูกออกซิเดชันในกรณีของโทลูอีนกลุ่มเมทิล MNO 2 ตัวออกซิไดเซอร์ออกซิไดซ์กับกลุ่ม Aldehyde, สารออกซิไดซ์ที่แข็งแกร่ง (KMNO 4) ทำให้เกิดการเกิดออกซิเดชันต่อไปที่กรด: 
นักเล่นเฆีนของเบนซีนใด ๆ ที่มีห่วงโซ่ด้านเดียวออกซิไดซ์โดยตัวแทนออกซิไดซ์ที่แข็งแกร่งของประเภท KMNO4 ในกรดเบนโซอิก I.e. การแยกโซ่ด้านข้างเกิดขึ้นกับการเกิดออกซิเดชันของส่วนวัยรุ่นของมันถึง CO 2; เช่น: 
ในการปรากฏตัวของโซ่ด้านข้างหลายตัวแต่ละตัวจะถูกออกซิไดซ์ไปยังกลุ่ม Carboxyl และกรดแบบ Polypic ที่เกิดขึ้นเช่น:

รับโทลูอีน:
ในอุตสาหกรรม:
1) การกลั่นน้ำมันและถ่านหิน
2) dehydrogenation ของ methylcyclohexane:

3) Heptane dehydrocyclication:
ในห้องปฏิบัติการ:
1) Alkylation ตาม Friedel Korfest;
2) ปฏิกิริยา Nureza Fittig (โซเดียมปฏิสัมพันธ์กับส่วนผสมของฮาโลเจนและฮาโลลีย์)
Arena (ไฮโดรคาร์บอนอะโรมาติก) – เหล่านี้เป็นไฮโดรคาร์บอนที่ไม่อิ่มตัว (ไม่อิ่มตัว) ที่มีโมเลกุลมีกลุ่มอะตอมที่มีเสถียรภาพของอะตอม (เคอร์เนลเบนซิน) ที่มีระบบปิดการเชื่อมต่อคอนจูเกต
สูตรทั่วไป: C N H 2N-6ที่ n ≥ 6
คุณสมบัติทางเคมี
อารีน่า- ไฮโดรคาร์บอนที่ไม่อิ่มตัวที่โมเลกุลมีสามพันธะและวงจรคู่ แต่เนื่องจากผลของการผันคำกริยาคุณสมบัติของเวทีแตกต่างจากคุณสมบัติของไฮโดรคาร์บอนที่ไม่มีค่าอื่น ๆ
สำหรับไฮโดรคาร์บอนอะโรมาติกปฏิกิริยาเป็นลักษณะ:
- การเข้าร่วม
- การแทน
- ออกซิเดชัน (สำหรับ benzene homologues)
ระบบอะโรมาติกของเบนซีนมีความทนทานต่อสารออกซิไดซ์ อย่างไรก็ตาม Benzene Homologs ถูกออกซิไดซ์ภายใต้การกระทำของโพแทสเซียมปรีดาและสารออกซิไดซ์อื่น ๆ
1. ปฏิกิริยาการเข้าร่วม
เบนซีนเข้าร่วมคลอรีนบนแสงและไฮโดรเจนเมื่อได้รับความร้อนในการปรากฏตัวของตัวเร่งปฏิกิริยา
1.1 การไฮโดรเจน
เบนซีนเข้าร่วมไฮโดรเจนเมื่อความร้อนและอยู่ภายใต้ความกดดันต่อการปรากฏตัวของตัวเร่งปฏิกิริยาโลหะ (NI, PT ฯลฯ )
เมื่อการเติมไฮโดรเจนของเบนซีนไซโคลเฮกเซนเกิดขึ้น:
เมื่อไฮโดรเนชันของ homologues, อนุพันธ์ cycloalkane เกิดขึ้น เมื่อโทลูอีนอุ่นด้วยไฮโดรเจนภายใต้ความกดดันและเมธิลไซคลีไซต์เกิดขึ้นในการปรากฏตัวของตัวเร่งปฏิกิริยา:
1.2 เวทีคลอรีน
การเพิ่มคลอรีนไปยังเบนซีน ในกลไกที่รุนแรงเมื่อ อุณหภูมิสูง ภายใต้การกระทำของรังสีอัลตราไวโอเลต
เมื่อคลอโร่เบนซีนแสงถูกสร้างขึ้น 1,2,3,4,5,6-Hexachlorcyclohexane (Hexahloran).
Hexakhloran - ยาฆ่าแมลงใช้ในการต่อสู้กับแมลงที่เป็นอันตราย ปัจจุบันห้ามใช้ Hexachlor เป็นสิ่งต้องห้าม
Gomezol Homologs ไม่ติดคลอรีน หากนักเดินเล่นเบนซินทำปฏิกิริยากับคลอรีนหรือโบรมีน บนแสงหรือที่อุณหภูมิสูง (300 ° C)จากนั้นมีการเปลี่ยนอะตอมไฮโดรเจน ใน alkyl substituent ด้านข้างและไม่ได้อยู่ในแหวนหอม
2. ปฏิกิริยาการทดแทน
2.1 ที่เยาะเย้ย
Benzole และ Homologs เข้าสู่ปฏิกิริยาของการทดแทนที่มีฮาลาโก (คลอรีนโบรมีน) ในการปรากฏตัวของตัวเร่งปฏิกิริยา (ALCL 3, Febre 3) .
เมื่อมีปฏิสัมพันธ์กับคลอรีนในตัวเร่งปฏิกิริยา ALCL 3 Chlorobenzene เกิดขึ้น:
ไฮโดรคาร์บอนอะโรมาติกมีปฏิสัมพันธ์กับโบรอมเมื่อได้รับความร้อนและต่อหน้าตัวเร่งปฏิกิริยา - Febre 3 เหล็กโลหะยังสามารถใช้เป็นตัวเร่งปฏิกิริยาได้
โบรมีนทำปฏิกิริยากับเหล็กในรูปแบบเหล็กโบรไมด์ (III) ซึ่งเร่งปฏิกิริยากระบวนการเช่าเบนซิน:
เมตา-Hlortoluol เกิดขึ้นในปริมาณเล็กน้อย
ในการโต้ตอบของ Gomologov Benzene ด้วย Halogens บนแสงหรือที่อุณหภูมิสูง (300 ° C) มีการทดแทนไฮโดรเจนไม่ได้อยู่ในแหวนเบนซิน แต่ในด้านข้างไฮโดรคาร์บอน
ตัวอย่างเช่นเมื่อ Chloroing Ethylbenzene:
2.2 ไนเตรท
Benzol ทำปฏิกิริยากับกรดไนตริกเข้มข้นในการปรากฏตัวของกรดซัลฟูริกเข้มข้น (ส่วนผสมเกลียว)
ในเวลาเดียวกัน nitrobenzene เกิดขึ้น:
โทลูอีนทำปฏิกิริยากับกรดไนตริกเข้มข้นในการปรากฏตัวของกรดซัลฟิวริกเข้มข้น
ในผลิตภัณฑ์ปฏิกิริยาเราระบุอย่างใดอย่างหนึ่ง เกี่ยวกับ-nithrololol:
หรือ p-nithrololol:
เกลียวของโทลูอีนสามารถไหลและเปลี่ยนอะตอมไฮโดรเจนสามอะตอม ในเวลาเดียวกัน 2,4,6-trinitrotoluolet (troil, tol) ถูกสร้างขึ้น:
2.3 Alkylation ของไฮโดรคาร์บอนอะโรมาติก
- Arena โต้ตอบกับ Halogens ในการปรากฏตัวของตัวเร่งปฏิกิริยา (ALCL 3, Febre 3 ฯลฯ ) ด้วยการก่อตัวของ Benzene Homologues
- ไฮโดรคาร์บอนอะโรมาติกมีปฏิสัมพันธ์กับอัลเคนในการปรากฏตัวของอลูมิเนียมคลอไรด์, เหล็กโบรไมด์ (III), กรดฟอสฟอริก, ฯลฯ
- แอลกอฮอล์ Alkylating เกิดขึ้นต่อหน้ากรดซัลฟิวริกเข้มข้น
2.4 ซัลโฟเนชันของไฮโดรคาร์บอนอะโรมาติก
Benzol ทำปฏิกิริยาเมื่อได้รับความร้อนด้วยกรดซัลฟิวริกเข้มข้นหรือ 3 โซลูชั่นในกรดซัลฟูริก (Oleum) ด้วยการก่อตัวของกรด Benzenesulfonic:
3. ออกซิเดชันของเวที
Benzole ทนต่อตัวแทนออกซิไดซ์ที่แข็งแกร่ง แต่ Benzol Homologs ถูกออกซิไดซ์ภายใต้การกระทำของสารออกซิไดซ์ที่แรง Benzole และ homologs ของเขากำลังไหม้อยู่
3.1. ออกซิเดชันเต็มรูปแบบ - การเผาไหม้
เมื่อการเผาไหม้เบนซีนและ homologs ของเขาเกิดขึ้น คาร์บอนไดออกไซด์ และน้ำ ปฏิกิริยาของการเผาไหม้ของเวทีนั้นมาพร้อมกับการเปิดตัวความร้อนจำนวนมาก
2C 6 H 6 + 15O 2 → 12CO 2 + 6H 2 O + Q
โดยทั่วไปสมการการเผาไหม้จะถูกแชร์:
C N H 2N-6 + (3N - 3) / 2 O 2 → NCO 2 + (N - 3) H 2 O + ถาม
ด้วยการเผาไหม้ไฮโดรคาร์บอนอะโรมาติกในข้อเสียของออกซิเจน COCHON MONOXIDE CO หรือ SAZH SAZ อาจเป็นแบบฟอร์ม
Benzole และ homologs ของเขาเผาไหม้ในอากาศด้วยเปลวไฟสูบบุหรี่ Benzole และ homologs รูปแบบการผสมผสานที่มีการระเบิดด้วยอากาศและออกซิเจน
3.2 เกี่ยวกับbenzol homologues เฉียบพลัน
Benzene Gomologists ได้รับการออกซิไดซ์ได้อย่างง่ายดายโดย Permanganate และโพแทสเซียม Dichromat ในสื่อที่เป็นกรดหรือเป็นกลางเมื่อได้รับความร้อน
ในเวลาเดียวกันเกิดขึ้น ออกซิเดชันการเชื่อมต่อทั้งหมดที่คาร์บอนอะตอม, บริเวณใกล้เคียงกับแหวนเบนซินยกเว้นการเชื่อมต่อของอะตอมคาร์บอนนี้กับแหวนเบนซิน
โทลูอีนถูกออกซิไดซ์ permanganate โพแทสเซียมในกรดซัลฟูริก ด้วยการศึกษา กรดเบนโซอิก:
หากออกซิเดชันของโทลูอีนไป ในสารละลายที่เป็นกลางเมื่อถูกความร้อนมันเกิดขึ้น เบนโซอิกกรดเกลือ - โพแทสเซียมเบนโซเอต:
ดังนั้นโทลูอีน การฆ่าเชื้อโพแทสเซียมปรกติอย่างเป็นกรด เมื่อถูกความร้อน
อนุมูลอิสระที่ออกซิไดซ์เป็นกรดเบนโซอิกและกรดคาร์บอกซิลิก:
เมื่อมีการก่อตัวเป็นโพรพิลแบ็นซีนออกซิไดซ์เบนโซอิกและกรดอะซิติก
Isopropyl Benzene ออกซิไดซ์โดยโพแทสเซียมปรีดาในสื่อที่เป็นกรดเป็นกรดเบนโซอิกและก๊าซคาร์บอนไดออกไซด์:
4. การปรับทิศทางการกระทำของแหล่งย่อยในแหวนเบนซิน
หากมีสารทดแทนในแหวนเบนซินไม่เพียง แต่อัลคิล แต่ยังมีอะตอมอื่น ๆ (ไฮดรอกซิล, อะมิโนกลุ่ม, nitroxyl, ฯลฯ ) ปฏิกิริยาของการเปลี่ยนอะตอมไฮโดรเจนในระบบอะโรมาติกดำเนินการอย่างเคร่งครัดในทางที่แน่นอน ด้วยธรรมชาติ อิทธิพลของสารทดแทนสำหรับระบบ acomatic π
ประเภทของแหล่งย่อยในแหวนเบนซิน
| รองผู้อำนวยการครั้งแรก Roda | รองผู้อำนวยการที่สอง Roda |
| ออร์โธ- ผม. คู่-ตำแหน่ง | การทดแทนเพิ่มเติมเกิดขึ้นส่วนใหญ่ใน เมตา-ตำแหน่ง |
| Electronium-term เพิ่มความหนาแน่นของอิเล็กทรอนิกส์ในแหวนเบนซิน | รถยนต์ไฟฟ้าประกอบลดความหนาแน่นของอิเล็กตรอนในระบบคอนจูเกต |
|
|
สมบัติทางกายภาพ
Benzole และ homologues ที่ใกล้ที่สุดเป็นของเหลวไม่มีสีที่มีกลิ่นที่เฉพาะเจาะจง ไฮโดรคาร์บอนอะโรมาติกมีน้ำหนักเบากว่าน้ำและไม่ละลายในนั้น แต่มันละลายได้ง่ายในตัวทำละลายอินทรีย์ - แอลกอฮอล์อีเธอร์อะซิโตน
เบนซีนและ homologs ของเขาเองเป็นตัวทำละลายที่ดีสำหรับสารอินทรีย์จำนวนมาก เวทีทั้งหมดกำลังลุกไหม้ด้วยเปลวไฟสูบบุหรี่เนื่องจากปริมาณคาร์บอนสูงของโมเลกุล Vik
คุณสมบัติทางกายภาพของเวทีบางอย่างจะถูกนำเสนอในตาราง
โต๊ะ. คุณสมบัติทางกายภาพของเวทีบางอย่าง
|
ชื่อ |
สูตร |
t °วาง, |
t ° .kip., |
|
เบนซีน |
c 6 h 6 |
5,5 |
80,1 |
|
โทลูอีน (methylbenzene) |
c 6 h 5 сh 3 |
95,0 |
110,6 |
|
เอทิลเบนซีน |
c 6 h 5 c 2 h 5 |
95,0 |
136,2 |
|
ไซลีน (Dimethylbenzene) |
C 6 H 4 (SH 3) 2 |
||
|
ortho- |
25,18 |
144,41 |
|
|
meta- |
47,87 |
139,10 |
|
|
คู่- |
13,26 |
138,35 |
|
|
Propillbenzene |
จาก 6 N 5 (CH 2) 2 CH 3 |
99,0 |
159,20 |
|
Kumol (Isopropylbenzene) |
c 6 h 5 ch (ch 3) 2 |
96,0 |
152,39 |
|
สไตรีน (Vinylbenzene) |
c 6 h 5 ch \u003d ch 2 |
30,6 |
145,2 |
เบนซีน - การต้มเบา ( ต. จิบ\u003d 80.1 ° C), ของเหลวไม่มีสี, ไม่ละลายในน้ำ
ความสนใจ! เบนซีน - พิษทำหน้าที่ในไตเปลี่ยนสูตรเลือด (ด้วยการเปิดรับแสงระยะยาว) อาจเป็นการละเมิดโครงสร้างของโครโมโซม
ไฮโดรคาร์บอนอะโรมาติกส่วนใหญ่เป็นอันตรายต่อชีวิตที่เป็นพิษ
การรับสนามกีฬา (เบนซีนและ homologues ของเขา)
ในห้องปฏิบัติการ
1. พื้นของเกลือกรดเบนโซอิกที่มีด่างแข็ง
C 6 H 5 -Coona + Naoh t →C 6 H 6 + NA 2 CO 3
โซเดียมเบนโซเอต
2. ปฏิกิริยาการติดตั้ง Nureza: (ที่นี่ g - ฮาโลเจน)
ด้วย 6เอช. 5 -g + 2นา. + อาร์-g →ค. 6 เอช. 5 - อาร์ + 2 นา.กรัม
จาก 6 H 5 -CL + 2NA + CH 3 -CL → C 6 H 5 -CH 3 + 2NACL
ในอุตสาหกรรม
- โดดเดี่ยวจากน้ำมันและถ่านหินโดยวิธีการกลั่นเศษส่วนปฏิรูป
- จากขดลวดเรซิ่นและก๊าซโค้ก
1. Alkanov Dehydrocyclication ด้วยจำนวนอะตอมคาร์บอนมากกว่า 6:
c 6 h 14 ต. , kat→ C 6 H 6 + 4H 2
2. การจอนของอะเซทิลีน (สำหรับเบนซินเท่านั้น) - อาร์ เกี่ยวกับ zelinsky:
3C 2. h 2. 600 ° ค. , พระราชบัญญัติ ถ่านหิน → C 6 H 6
3. การทำให้แห้ง ไซโคลเฮกเซนและ homologues ของเขา:
นักวิชาการโซเวียต Nikolai Dmitrievich Zelinsky พบว่าเบนซีนเกิดขึ้นจาก Cyclohexane (Cycloalkan Dehydrogenation
c 6 h 12 t, kat→ C 6 H 6 + 3H 2

c 6 h 11 -ch 3 ต. , kat→ C 6 H 5 -CH 3 + 3H 2
methylcyclohexantoluole
4. Alkylation ของเบนซีน (การได้รับ Gomologists เบนซีน) - r freidel korflas.
c 6 h 6 + c 2 h 5 -cl t, alcl3→ C 6 H 5 -C 2 H 5 + HCL
chlorhetan เอทิลเบนซีน

คุณสมบัติทางเคมี
ผม.. ปฏิกิริยาออกซิเดชั่น
1. การเผาไหม้ (เปลวไฟสูบบุหรี่):
2c 6 h 6 + 15o 2 ต. → 12CO 2 + 6H 2 O + Q
2. Benzole ภายใต้สภาวะปกติไม่เปลี่ยนสีน้ำโบรมีนและสารละลายน้ำของแมงกานีส
3. Benzol Homologs ถูกออกซิไดซ์โดยโพแทสเซียมปรีดา (เปลี่ยนสีโดยแมงกานีส):
a) ในสื่อที่เป็นกรดเป็นกรดเบนโซอิก
ภายใต้การดำเนินการกับ Gomologists ของ Potassium Permanganate และสารออกซิไดซ์อื่น ๆ โซ่ด้านข้างออกซิไดซ์ ไม่ว่าห่วงโซ่ของสารทดแทนจะยากแค่ไหนมันถูกทำลายยกเว้น - Aatoma Carbon ซึ่งออกซิไดซ์ในกลุ่ม Carboxyl
Gomezol Homologs ที่มีห่วงโซ่ด้านเดียวให้กรดเบนโซอิก:
homologists ที่มีโซ่สองด้านให้กรดสองแกน:
5c 6 h 5 -c 2 h 5 + 12kmno 4 + 18h 2 ดังนั้น 4 → 5c 6 h 5 coh + 5co 2 + 6k 2 ดังนั้น 4 + 12mnso 4 + 28h 2 o
5c 6 h 5 -ch 3 + 6kmno 4 + 9h 2 ดังนั้น 4 → 5c 6 h 5 coh + 3k 2 ดังนั้น 4 + 6mnso 4 + 14h 2 o
ง่ายขึ้น :
c 6 h 5 -ch 3 + 3o KMNO4→ C 6 H 5 Coh + H 2 O
b) ในที่เป็นกลางและอัลคาไลน์ต่ำถึงเกลือกรดเบนโซอิก
C 6 H 5 -CH 3 + 2KMNO 4 → C 6 H 5 COOk + k เขา + 2mno 2 + h 2 o
ครั้งที่สอง. ปฏิกิริยาของการเข้าร่วม (หนักกว่าอัลเคน)
1. ฮาโลเจน
C 6 H 6 + 3CL 2 เอช. ν → C 6 H 6 CL 6 (Hexakhlorcyclohexane - Hexakhloran)
2. ไฮโดรจิเนชัน
C 6 H 6 + 3H 2 ต. , pt. หรือ ni → C 6 H 12 (Cyclohexane)
3. พอลิเมอร์
สาม. ปฏิกิริยาการทดแทน - กลไกไอออน (เบากว่า Alkanov)
1. ฮาโลเจน -
ก. ) เบนซอล
C 6 H 6 + CL 2 alcl 3 → C 6 H 5 -CL + HCL (คลอโรเบนซีน)
C 6 H 6 + 6CL 2 t, alcl3→ C 6 CL 6 + 6HCL( hexakhlorbenzene)
c 6 h 6 + br 2 t, fecl3→ C 6 H 5 -BR + HBR( bromboenzene)
b) benzene homologues ในระหว่างการฉายรังสีหรือความร้อน
โดยคุณสมบัติทางเคมีอนุมูลอัลคิลมีความคล้ายคลึงกับ Alkanes อะตอมไฮโดรเจนในพวกเขาถูกแทนที่ด้วยฮาโลเจนในกลไกที่อนุมานฟรี ดังนั้นในกรณีที่ไม่มีตัวเร่งปฏิกิริยาระหว่างการทำความร้อนหรือการฉายรังสียูวีปฏิกิริยาที่รุนแรงของการทดแทนในห่วงโซ่ด้านข้างกำลังดำเนินการอยู่ ผลกระทบของแหวนเบนซินในการแทนที่อัลคิลนำไปสู่ความจริงที่ว่า อะตอมไฮโดรเจนที่อะตอมคาร์บอนมักเกี่ยวข้องโดยตรงกับแหวนเบนซิน (A - AATOMA ของคาร์บอน) จะถูกแทนที่
1) C 6 H 5 -CH 3 + CL 2 เอช. ν → C 6 H 5 -CH 2 -CL + HCL
c) benzene homologues ต่อหน้าตัวเร่งปฏิกิริยา
c 6 h 5 -ch 3 + cl 2 alcl 3 → (ส่วนผสมของ ORTA, คู่ตราสารอนุพันธ์) + hcl
2. สารอาหาร (มีกรดไนตริก)
c 6 h 6 + ho-no 2 t, h2so4→ C 6 H 5 -NO 2 + H 2 O
nitrobenzene - กลิ่น อัลมอนด์!
c 6 h 5 -ch 3 + 3ho-no 2 t, h2so4→ จาก H 3 -C 6 H 2 (NO 2) 3 + 3H 2 O2,4,6-trinitroluole (tol, trotil)
การใช้เบนซีนและ homologues ของเขา
เบนซีน c 6 h 6 เป็นตัวทำละลายที่ดี Benzole เป็นสารเติมแต่งช่วยปรับปรุงคุณภาพของเชื้อเพลิงมอเตอร์ ทำหน้าที่เป็นวัตถุดิบที่จะได้รับสารประกอบอินทรีย์ที่มีกลิ่นหอมมากมาย - Nitrobenzene C 6 H 5 NO 2 (ตัวทำละลาย, Aniline ได้รับจากมัน), Chlorobenzene C 6 h 5 cl, ฟีนอลซี 6 h 5 โอ้สไตรีน ฯลฯ
โทลูอีน C 6 H 5 -CH 3 เป็นตัวทำละลายที่ใช้ในการผลิตสีย้อมสมุนไพรและวัตถุระเบิด (Trotil (TOL) หรือ 2,4,6-Trinitrotrol Tilt)
ไซลีนC 6 H 4 (CH 3) 2. Xylene ทางเทคนิค - ส่วนผสมของสามไอโซเมอร์ ( ออร์โธ-, เมตา- ผม. คู่-XILOLOV) - ใช้เป็นตัวทำละลายและผลิตภัณฑ์ต้นทางสำหรับการสังเคราะห์สารประกอบอินทรีย์จำนวนมาก
isopropylbenzene C 6 H 5 -CH (CH 3) 2 ทำหน้าที่รับฟีนอลและอะซิโตน
เบนซอลอนุพันธ์คลอโร ใช้เพื่อป้องกันพืช ดังนั้นผลิตภัณฑ์ทดแทนในเบนซีนอะตอม n อะตอมคลอรีน - Hexachlorobenzene ที่มี 6 cl 6 - ยาฆ่าเชื้อรา; มันถูกใช้สำหรับการแกะสลักเมล็ดพันธุ์ข้าวสาลีแห้งและไรย์กับหัวทึบ การเพิ่มผลิตภัณฑ์ของคลอรีนกับเบนซีน - Hexachlorcyclohexane (Hexachlororan) ที่มี 6 ชั่วโมง 6 cl 6 - ยาฆ่าแมลง; มันถูกใช้เพื่อต่อสู้กับแมลงที่เป็นอันตราย สารเหล่านี้เกี่ยวข้องกับสารกำจัดศัตรูพืช - เคมีภัณฑ์เพื่อต่อสู้กับจุลินทรีย์พืชและสัตว์
สไตรีน c 6 h 5 - ch \u003d ch 2 เป็นโพลีสไตรีนที่สร้างขึ้นได้ง่ายมากและ copolymery กับ butadiene - butadienestrol ยาง
การทดลองวิดีโอ